Fensiklidina atau fenilsikloheksil piperidina (PCP), yang juga dikenal dalam penggunaannya sebagai narkoba jalanan dengan nama angel dust di antara nama-nama lainnya, adalah sebuah obat anestesi disosiatif yang utamanya digunakan secara rekreasional karena efeknya yang signifikan dalam mengubah kesadaran. PCP dapat menyebabkan halusinasi, distorsi persepsi suara, dan perilaku psikotik. Sebagai narkoba rekreasional, obat ini biasanya dibakar/dihisap, tetapi dapat juga dikonsumsi melalui mulut, dihirup melalui hidung, atau disuntikkan. Obat ini juga dapat dicampur dengan kanabis atau tembakau.
Sumber: Lihat artikel asli di Wikipedia

Artikel ini membahas mengenai narkotika, psikotropika, dan zat adiktif lainnya. Informasi mengenai zat dan obat-obatan terlarang hanya dimuat demi kepentingan ilmu pengetahuan. Kepemilikan dan pengedaran narkoba adalah tindakan melanggar hukum di berbagai negara. Baca: penyangkalan umum lihat pula: nasihat untuk orang tua. |
 | |
 | |
| Data klinis | |
|---|---|
| Nama dagang | Sernyl, Sernylan (keduanya sudah dihentikan) |
| Nama lain | CI-395; Phenylcyclohexylpiperidine; "Angel dust"[1] |
| AHFS/Drugs.com | entry |
| Potensi ketergantungan | Fisik: Rendah Psikologis: Sedang[2] |
| Potensi kecanduan | Bervariasi, dilaporkan dari rendah hingga tinggi[2][3] |
| Rute pemberian | Merokok, injeksi, dihirup, melalui mulut[4][5] |
| Kelas obat | Antagonis reseptor NMDA; Anestesi umum; Halusinogen disosiatif[4] |
| Kode ATC |
|
| Status hukum | |
| Status hukum |
|
| Data farmakokinetika | |
| Metabolisme | Hidroksilasi oksidatif di hati oleh enzim CYP450, glukuronidasi |
| Metabolit | PCHP, PPC, PCAA |
| Onset aksi | 2–60 menit[6] |
| Waktu paruh eliminasi | 7–46 jam |
| Durasi aksi | 6–48 jam[6] |
| Ekskresi | Urin |
| Pengenal | |
| |
| Nomor CAS |
|
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank |
|
| ChemSpider |
|
| UNII | |
| KEGG |
|
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.150.427 |
| Data sifat kimia dan fisik | |
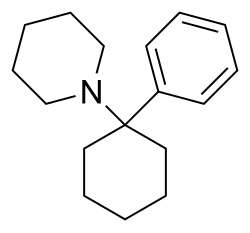
| Rumus | C17H25N |
| Massa molar | 243,39 g·mol−1 |
| Model 3D (JSmol) | |
| Titik leleh | 465 °C (869 °F) |
| Titik didih | 136 °C (277 °F) |
| |
| |
| | |
Fensiklidina atau fenilsikloheksil piperidina (PCP), yang juga dikenal dalam penggunaannya sebagai narkoba jalanan dengan nama angel dust di antara nama-nama lainnya, adalah sebuah obat anestesi disosiatif yang utamanya digunakan secara rekreasional karena efeknya yang signifikan dalam mengubah kesadaran.[4][1] PCP dapat menyebabkan halusinasi, distorsi persepsi suara, dan perilaku psikotik.[4][7][8] Sebagai narkoba rekreasional, obat ini biasanya dibakar/dihisap, tetapi dapat juga dikonsumsi melalui mulut, dihirup melalui hidung, atau disuntikkan.[4][5][7] Obat ini juga dapat dicampur dengan kanabis atau tembakau.[4][1]
Efek samping dapat mencakup paranoia, kecanduan, dan peningkatan risiko bunuh diri, serta kejang dan koma dalam kasus overdosis.[7] Flashback dapat terjadi meskipun penggunaan telah dihentikan.[8] Secara kimiawi, PCP adalah anggota dari kelas arilsikloheksilamina.[4][9][10] PCP bekerja terutama sebagai Antagonis reseptor NMDA.[9]
PCP paling umum digunakan di Amerika Serikat.[11] Meskipun penggunaannya mencapai puncak di AS pada tahun 1970-an,[12] antara tahun 2005 dan 2011, terjadi peningkatan kunjungan ke unit gawat darurat sebagai akibat dari obat ini.[7] Hingga tahun 2022, di AS, sekitar 0,7% siswa kelas 12 melaporkan menggunakan PCP dalam setahun terakhir, sementara 1,7% orang di AS di atas usia 25 tahun melaporkan menggunakannya pada suatu saat dalam hidup mereka.[13]

Fensiklidin digunakan karena kemampuannya untuk menginduksi keadaan disosiatif.[14]
Efek perilaku dapat bervariasi berdasarkan dosis. Dosis rendah menghasilkan mati rasa pada anggota gerak dan intoksikasi, yang ditandai dengan jalan sempoyongan, gaya berjalan tidak stabil, bicara cadel, mata merah, dan hilangnya keseimbangan. Dosis sedang (5–10 mg intranasal, atau 0,01–0,02 mg/kg intramuskular atau intravena) akan menghasilkan analgesia dan anestesi. Dosis tinggi dapat menyebabkan kejang.[15] Obat ini sering diproduksi secara ilegal dalam kondisi yang kurang terkontrol; hal ini membuat pengguna mungkin tidak menyadari dosis aktual yang mereka konsumsi.[16]
Efek psikologis meliputi perubahan parah pada citra tubuh, hilangnya batasan ego, paranoia, dan depersonalisasi. Psikosis, agitasi dan disforia, halusinasi, penglihatan kabur, euforia, dan dorongan bunuh diri juga dilaporkan, serta sesekali perilaku agresif.[15][17][18]: 48–49 PCP dapat menginduksi perasaan kuat, berkuasa, dan tak terkalahkan serta efek mati rasa pada pikiran.[5]
Studi oleh Drug Abuse Warning Network pada tahun 1970-an menunjukkan bahwa laporan media tentang kekerasan akibat PCP sangat dilebih-lebihkan dan insiden kekerasan jarang terjadi, sering kali terbatas pada individu yang memiliki reputasi agresif terlepas dari penggunaan obat.[18]: 48 Meskipun jarang, kejadian individu yang terintoksikasi PCP bertindak secara tak terduga, kemungkinan didorong oleh delusi atau halusinasi mereka, telah dipublikasikan.[19] Jenis insiden lain yang umum dikutip termasuk merusak properti dan berbagai jenis mutilasi diri, seperti mencabut gigi sendiri.[18]: 48 [19] Efek-efek ini tidak dicatat dalam penggunaan medisnya pada tahun 1950-an dan 1960-an, tetapi, laporan kekerasan fisik pada PCP sering kali terbukti tidak berdasar.[20][21]
Dosis rekreasional obat ini juga terkadang tampak menginduksi keadaan psikotik, dengan gangguan emosional dan kognitif yang menyerupai episode skizofrenia.[22][23] Pengguna umumnya melaporkan merasa terpisah dari kenyataan.[24]
Gejala diringkas dengan jembatan keledai RED DANES: rage (kemarahan), eritema (kemerahan pada kulit), pupil melebar (dilated pupils), delusi, amnesia, nistagmus (osilasi bola mata saat bergerak ke samping), eksitasi, dan kulit kering.[25]
PCP diberikan secara mandiri dan menginduksi ekspresi ΔFosB pada neuron spiny medium tipe D1 di nukleus akumbens,[3][26] dan karenanya, penggunaan PCP berlebihan diketahui menyebabkan kecanduan.[3] Efek penghargaan (rewarding) dan penguatan (reinforcing) PCP setidaknya sebagian dimediasi oleh pemblokiran reseptor NMDA pada input glutamatergik ke neuron spiny medium tipe D1 di nukleus akumbens.[3] PCP telah terbukti menghasilkan keengganan tempat terkondisi (conditioned place aversion) dan preferensi tempat terkondisi (conditioned place preference) dalam studi hewan.[27]
Tinjauan tahun 2019 menemukan bahwa tingkat transisi dari diagnosis psikosis akibat halusinogen (termasuk PCP) ke skizofrenia adalah 26%. Angka ini lebih rendah daripada psikosis akibat kanabis (34%) tetapi lebih tinggi daripada psikosis akibat amfetamin (22%), opioid (12%), alkohol (10%), dan sedatif (9%). Sebagai perbandingan, tingkat transisi ke skizofrenia untuk psikosis "singkat, atipikal, dan tidak ditentukan lain" ditemukan sebesar 36%.[28]
PCP memiliki beberapa rute pemberian. Paling umum, bentuk bubuk dari obat ini dihirup melalui hidung (snorted). PCP juga dapat ditelan secara oral, disuntikkan secara subkutan atau intravena, atau diisap bersama ganja atau rokok.[29]
Penanganan intoksikasi PCP sebagian besar terdiri dari perawatan suportif – mengendalikan pernapasan, sirkulasi, dan suhu tubuh – serta, pada tahap awal, menangani gejala psikiatri.[31][32][33] Benzodiazepin, seperti lorazepam, merupakan obat pilihan untuk mengendalikan agitasi dan kejang (jika ada). Antipsikotik tipikal seperti fenotiazina dan haloperidol pernah digunakan untuk mengendalikan gejala psikotik, tetapi dapat menimbulkan banyak efek samping yang tidak diinginkan – seperti distonia – sehingga penggunaannya tidak lagi diutamakan; fenotiazina sangat berisiko karena dapat menurunkan ambang kejang, memperburuk hipertermia, dan meningkatkan efek antikolinergik dari PCP.[31][32] Jika antipsikotik diberikan, haloperidol melalui injeksi intramuskular telah direkomendasikan.[33][34][35]
Diuresis asam paksa (dengan amonium klorida atau, yang lebih aman, asam askorbat) dapat meningkatkan pembersihan PCP dari tubuh, dan pada masa lalu sempat direkomendasikan secara kontroversial sebagai langkah dekontaminasi.[31][32][33] Namun, sekarang diketahui bahwa hanya sekitar 10% dari dosis PCP yang dikeluarkan melalui ginjal, yang membuat peningkatan pembersihan melalui urin tidak memberikan dampak yang berarti; selain itu, pengasaman urin berbahaya karena dapat memicu asidosis dan memperburuk rabdomiolisis (kerusakan otot), yang merupakan manifestasi umum dari toksisitas PCP.[31][32]
| Situs | Ki (nM) | Aksi | Spesies | Ref |
|---|---|---|---|---|
| NMDA | 59 | Antagonis | Manusia | [38] |
| MOR | >10.000 | ND | Manusia | [38] |
| DOR | >10.000 | ND | Manusia | [38] |
| KOR | >10.000 | ND | Manusia | [38] |
| NOP | >10.000 | ND | Manusia | [38] |
| σ1 | >10.000 | Agonis | Marmut | [38][39] |
| σ2 | 136 | Agonis | Tikus | [38] |
| D2 | >10.000 | ND | Manusia | [38] |
| D2High | 2,7–4,3 144 (EC50) | Agonis Parsial | Tikus/manusia Manusia | [40][41] [42] |
| 5-HT2A | >10.000 | ND | Manusia | [38] |
| 5-HT2AHigh | ≥5.000 | Agonis Parsial | Tikus | [41][43] |
| SERT | 2.234 | Inhibitor | Manusia | [38] |
| NET | >10.000 | Inhibitor | Manusia | [38] |
| DAT | >10.000 | Inhibitor | Manusia | [38] |
| PCP2 | 154 | agonis | Manusia | [44] |
| Ambilan [3H]5-HT | 1.424 (IC50) | Inhibitor | Tikus | [45] |
| Ikatan [3H]NIS | 16.628 (IC50) | Inhibitor | Tikus | [45] |
| Ambilan [3H]DA | 347 (IC50) | Inhibitor | Tikus | [45] |
| Ikatan [3H]CFT | 1.547 (IC50) | Inhibitor | Tikus | [45] |
| Nilai adalah Ki (nM). Semakin kecil nilainya, semakin kuat obat berikatan dengan situs tersebut. | ||||
PCP dikenal luas karena aksi utamanya pada reseptor NMDA, sebuah reseptor glutamat ionotropik.[46] Dengan demikian, PCP adalah sebuah antagonis reseptor NMDA non-kompetitif. Peran antagonisme NMDAR dalam efek PCP, ketamin, dan agen disosiatif terkait pertama kali dipublikasikan pada awal 1980-an oleh David Lodge dan rekan-rekan.[47] Antagonis reseptor NMDA lainnya meliputi ketamin, tiletamina, dekstrometorfan, dinitrogen oksida, dan dizosilpin (MK-801).
Penelitian juga menunjukkan bahwa PCP menghambat reseptor asetilkolin nikotinik (nAChRs) di antara mekanisme lainnya. Analog dari PCP menunjukkan potensi yang bervariasi pada reseptor nACh dan reseptor NMDA. Temuan menunjukkan bahwa interaksi nAChRs prasinaps dan reseptor NMDA memengaruhi pematangan pascasinaps dari sinapsis glutamatergik dan akibatnya berdampak pada perkembangan serta plastisitas sinaptik di otak. Efek-efek ini dapat menyebabkan penghambatan aktivitas glutamat eksitatorik di wilayah otak tertentu seperti hipokampus dan otak kecil, sehingga berpotensi menyebabkan hilangnya ingatan sebagai salah satu efek penggunaan jangka panjang. Efek akut pada otak kecil bermanifestasi sebagai perubahan tekanan darah, laju pernapasan, laju nadi, dan hilangnya koordinasi otot selama intoksikasi.[8]
PCP, seperti ketamin, juga bertindak sebagai agonis parsial reseptor dopamin D2High yang poten pada homogenat otak tikus dan memiliki afinitas terhadap reseptor D2High manusia yang dikloning. Aktivitas ini mungkin terkait dengan beberapa fitur psikotik lainnya dari intoksikasi PCP, yang dibuktikan dengan keberhasilan penggunaan antagonis reseptor D2 (seperti haloperidol) dalam pengobatan psikosis PCP.
Selain interaksinya yang telah dieksplorasi dengan reseptor NMDA, PCP juga terbukti menghambat ambilan kembali dopamin, dan dengan demikian menyebabkan peningkatan kadar dopamin ekstraseluler sehingga meningkatkan neurotransmisi dopaminergik. Namun, PCP memiliki sedikit afinitas terhadap transporter monoamina manusia, termasuk transporter dopamin (DAT). Sebaliknya, penghambatan ambilan kembali monoamina yang dilakukannya mungkin dimediasi oleh interaksi dengan situs alosterik pada transporter monoamina. PCP merupakan ligan afinitas tinggi bagi situs PCP 2 (Ki = 154 nM), sebuah situs yang belum terkarakterisasi dengan baik yang dikaitkan dengan penghambatan ambilan kembali monoamina.
Studi pada tikus menunjukkan bahwa PCP berinteraksi secara tidak langsung dengan reseptor opioid (endorfin dan ensefalin) untuk menghasilkan analgesia.
Sebuah studi pengikatan menilai PCP pada 56 situs termasuk reseptor neurotransmiter dan transporter, menemukan bahwa PCP memiliki nilai Ki >10.000 nM pada semua situs kecuali situs dizosilpin (MK-801) dari reseptor NMDA (Ki = 59 nM), reseptor σ2 (Ki = 136 nM), dan transporter serotonin (Ki = 2.234 nM). Hasil ini menunjukkan bahwa PCP adalah ligan yang sangat selektif untuk NMDAR dan reseptor σ2. Namun, PCP juga dapat berinteraksi dengan situs alosterik pada transporter monoamina untuk menghasilkan penghambatan ambilan kembali monoamina.
Fensiklidin adalah antagonis reseptor NMDA non-kompetitif yang menghambat aktivitas reseptor NMDA untuk menyebabkan anestesi dan analgesia tanpa menyebabkan depresi kardiorespirasi.[17][48] NMDA adalah reseptor eksitatorik di otak; ketika diaktivasi secara normal, reseptor tersebut bertindak sebagai saluran ion dan terjadi aliran masuk ion positif melalui saluran untuk menyebabkan depolarisasi sel saraf. Fensiklidin menghambat reseptor NMDA dengan berikatan pada situs pengikatan PCP spesifik yang terletak di dalam saluran ion.[49] Situs pengikatan PCP berada di dekat situs pemblokiran magnesium, yang mungkin menjelaskan efek penghambatan yang serupa.[50]
Pengikatan pada situs PCP dimediasi oleh dua interaksi non-kovalen di dalam reseptor: ikatan hidrogen dan interaksi hidrofobik.[51] Pengikatan juga dikendalikan oleh mekanisme gerbang (gating) saluran ion. Karena situs PCP terletak di dalam saluran ion, ko-agonis seperti glisina harus berikatan dan membuka saluran agar PCP dapat masuk, berikatan dengan situs PCP, dan memblokir saluran tersebut.[52]
Beberapa studi menemukan bahwa, seperti antagonis reseptor NMDA lainnya, PCP dapat menyebabkan sejenis kerusakan otak yang disebut Lesi Olney pada tikus.[53] Studi yang dilakukan pada tikus menunjukkan bahwa dosis tinggi antagonis reseptor NMDA dizosilpin menyebabkan terbentuknya vakuola reversibel di wilayah tertentu pada otak tikus. Semua studi tentang lesi Olney hanya dilakukan pada hewan non-manusia dan mungkin tidak berlaku bagi manusia. Satu studi yang tidak dipublikasikan oleh Frank Sharp dilaporkan menunjukkan tidak ada kerusakan oleh antagonis NMDA ketamin (obat yang secara struktural serupa) jauh di atas dosis rekreasional, tetapi karena studi tersebut tidak pernah diterbitkan, validitasnya masih kontroversial.
PCP juga terbukti menyebabkan perubahan kadar N-asetilaspartat dan N-asetilaspartilglutamat di otak tikus yang menyerupai skizofrenia, yang dapat dideteksi baik pada tikus hidup maupun melalui pemeriksaan nekropsi jaringan otak.[54] Obat ini juga menginduksi gejala pada manusia yang meniru skizofrenia.[55]
PCP tidak hanya menghasilkan gejala yang mirip dengan skizofrenia, tetapi juga menghasilkan perubahan elektroensefalogram pada jalur talamokortikal (peningkatan delta, penurunan alpha) dan di hipokampus (peningkatan letupan theta) yang serupa dengan yang ditemukan pada penderita skizofrenia.[56] Augmentasi pelepasan dopamin yang diinduksi PCP dapat menghubungkan hipotesis NMDA dan dopamin mengenai skizofrenia.[57]

PCP larut dalam air maupun lemak, sehingga terdistribusi ke seluruh tubuh dengan cepat.[50] PCP dimetabolisme menjadi PCHP, PPC, dan PCAA. Sebanyak 90% obat ini dimetabolisme melalui hidroksilasi oksidatif di hati selama metabolisme lintas pertama. Metabolit tersebut kemudian mengalami glukuronidasi dan diekskresikan dalam urin. Sembilan persen PCP yang tertelan diekskresikan dalam bentuk yang tidak berubah.[17]
Saat diisap (seperti rokok), sebagian senyawa terurai oleh panas menjadi 1-fenilsikloheksena (PC) dan piperidina.
Waktu yang dibutuhkan sebelum efek PCP bermanifestasi bergantung pada rute pemberiannya. Awitan kerja (onset) untuk inhalasi terjadi dalam 2–5 menit, sedangkan efeknya mungkin membutuhkan waktu 15 hingga 60 menit jika tertelan secara oral.[17]
PCP adalah sebuah arilsikloheksilamina.

Kurang dari 30 analog struktural PCP yang berbeda dilaporkan telah digunakan sebagai narkoba jalanan selama tahun 1970-an dan 1980-an, terutama di Amerika Serikat.[58] Hanya beberapa dari senyawa ini yang digunakan secara luas, termasuk rolisiklidina (PCPy), etisiklidina (PCE), dan tenosiklidina (TCP).[58] Analog yang kurang umum meliputi 3-HO-PCP, 3-MeO-PCMo, dan 3-MeO-PCP.
Motif struktural umum yang diperlukan untuk aktivitas serupa PCP diturunkan dari studi hubungan struktur-aktivitas dari turunan PCP. Semua turunan ini kemungkinan besar memiliki kesamaan efek psikoaktif dengan PCP itu sendiri, meskipun berbagai tingkat potensi dan variasi campuran efek anestesi, disosiatif, dan stimulan telah diketahui, tergantung pada obat tertentu dan substituennya. Di Amerika Serikat, semua senyawa ini akan dianggap sebagai analog zat terkendali dari PCP di bawah Federal Analog Act dan karenanya merupakan obat-obatan terlarang jika dijual untuk konsumsi manusia.[59][60]
Fensiklidin awalnya ditemukan pada tahun 1926 oleh Arthur Kötz dan mahasiswanya Paul Merkel sebagai produk dari reaksi Grignard 1-piperidinosikloheksankarbonitril.[61]
Senyawa ini disintesis kembali pada tahun 1956 oleh kimiawan H. Victor Maddox dan dipasarkan sebagai obat anestetik oleh perusahaan farmasi Parke-Davis, yang sekarang merupakan anak perusahaan Pfizer.[10][56][61][62][63] Penggunaannya pada manusia dilarang di AS pada tahun 1965 karena tingginya tingkat efek samping, sementara penggunaannya pada hewan dilarang pada tahun 1978.[1][10][64] Terlebih lagi, ketamin telah ditemukan dan memiliki toleransi yang lebih baik sebagai anestetik.[64]
PCP diklasifikasikan sebagai obat golongan II (schedule II) di AS.[1] Turunan dari PCP telah dijual untuk penggunaan rekreasional dan non-medis.[58]
PCP adalah zat Golongan II di AS. Administrative Controlled Substances Code Number (ACSCN) untuk PCP adalah 7471.[65] Kuota produksinya untuk tahun 2014 adalah 19 gram (0,67 oz).[66] Obat ini termasuk narkotika Golongan I berdasarkan Undang-Undang Obat dan Zat Terkendali di Kanada, obat Daftar I dalam Undang-Undang Opium di Belanda, dan zat Kelas A di Inggris.[67]
PCP mulai muncul sebagai obat rekreasional di kota-kota besar di AS pada tahun 1960-an.[7] Pada tahun 1978, majalah People dan Mike Wallace dari program berita TV 60 Minutes menyebut PCP sebagai "masalah narkoba nomor satu" di negara tersebut. Meskipun penggunaan rekreasional obat ini sebenarnya selalu relatif rendah, jumlahnya mulai menurun secara signifikan pada tahun 1980-an. Dalam survei, jumlah siswa SMA yang mengaku pernah mencoba PCP setidaknya sekali turun dari 13% pada tahun 1979 menjadi kurang dari 3% pada tahun 1990.[18]: 46–49
Jean-Michel Basquiat menggambarkan dua pengguna angel dust dalam lukisannya yang dibuat pada tahun 1982 berjudul Dustheads.[68]
Manga karya Tsukasa Hojo tahun 1985, City Hunter, menampilkan sebuah obat bernama "Angel Dust", yang kemungkinan merujuk pada nama jalanan PCP. Film animasi tahun 2023 yang terkait, City Hunter: Angel Dust, membawa istilah ini lebih jauh ke ranah fantasi, di mana ia digambarkan sebagai serum nanomesin fiksi ilmiah yang dikembangkan oleh perusahaan bioteknologi untuk menciptakan tentara super dengan kecenderungan menjadi mengamuk (berserk), menjauh dari fakta PCP di dunia nyata.[69]
Di lokasi syuting film Titanic, lebih dari 80 kru jatuh sakit dalam satu hari. Sejumlah ambulans tiba di lokasi selama beberapa jam untuk membawa para pekerja film tersebut satu per satu. Ternyata seseorang telah melakukan lelucon kejam dan mencampur sup lobster bisque dengan PCP. Pelakunya tidak pernah teridentifikasi.
high abuse liability
PCP can lead to hostile behavior that may result in episodes of extreme violence