Talium(III) oksida adalah sebuah senyawa anorganik dari talium dan oksigen dengan rumus kimia Tl2O3. Senyawa ini terdapat di alam sebagai mineral langka avisenit. Strukturnya memiliki keterkaitan dengan Mn2O3 yang memiliki struktur seperti biksbyit. Tl2O3 bersifat metalik dengan konduktivitas tinggi dan merupakan semikonduktor tipe-n yang terdegenerasi yang berpotensi digunakan dalam sel surya. Metode untuk memproduksi Tl2O3 melalui MOCVD telah diketahui. Setiap penggunaan praktis dari talium(III) oksida harus selalu memperhitungkan sifat beracun talium. Kontak dengan kelembapan dan asam dapat membentuk senyawa talium yang beracun.
Sumber: Lihat artikel asli di Wikipedia

 | |
| Nama | |
|---|---|
| Nama lain
Talium trioksida Talium seskuioksida Tali oksida | |
| Penanda | |
Model 3D (JSmol) |
|
| ChemSpider |
|
| Nomor EC | |
PubChem CID |
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA) |
|
| |
| |
| Sifat[1] | |
| Tl2O3 | |
| Massa molar | 456,76 g/mol |
| Penampilan | Padatan cokelat gelap |
| Densitas | 10,19 g/cm3, padatan (22 °C) |
| Titik lebur | 717 °C (1.323 °F; 990 K) |
| Titik didih | 875 °C (1.607 °F; 1.148 K) (terdekomposisi) |
| Tak larut | |
| +76,0·10−6 cm3/mol | |
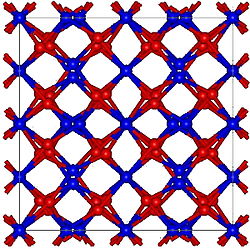
| Struktur | |
| Kubik, (biksbyit) cI80[2] | |
| Ia3 (No. 206) | |
| Bahaya | |
| Piktogram GHS |    |
| Keterangan bahaya GHS | {{{value}}} |
| H373, H411 | |
| P273, P314 | |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median) |
44 mg/kg (oral, tikus) |
| Senyawa terkait | |
Kation lainnya |
Talium(I) oksida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Talium(III) oksida adalah sebuah senyawa anorganik dari talium dan oksigen dengan rumus kimia Tl2O3. Senyawa ini terdapat di alam sebagai mineral langka avisenit.[3] Strukturnya memiliki keterkaitan dengan Mn2O3 yang memiliki struktur seperti biksbyit. Tl2O3 bersifat metalik dengan konduktivitas tinggi dan merupakan semikonduktor tipe-n yang terdegenerasi yang berpotensi digunakan dalam sel surya.[4] Metode untuk memproduksi Tl2O3 melalui MOCVD telah diketahui.[5] Setiap penggunaan praktis dari talium(III) oksida harus selalu memperhitungkan sifat beracun talium. Kontak dengan kelembapan dan asam dapat membentuk senyawa talium yang beracun.
Senyawa ini diproduksi melalui reaksi talium dengan oksigen atau hidrogen peroksida dalam larutan talium(I) yang bersifat basa. Atau, senyawa ini dapat dibuat melalui oksidasi talium(I) nitrat oleh klorin dalam larutan kalium hidroksida berair.[6]