Osimertinib adalah obat yang digunakan untuk mengobati karsinoma paru non-sel kecil dengan mutasi spesifik. Obat ini adalah penghambat tirosin kinase reseptor faktor pertumbuhan epidermal generasi ketiga.
Sumber: Lihat artikel asli di Wikipedia
 | |
| Data klinis | |
|---|---|
| Nama dagang | Tagrisso, dll |
| Nama lain | Templat:Infobox drug/localINNvariants |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a616005 |
| License data |
|
| Kategori kehamilan |
|
| Rute pemberian | Oral |
| Kode ATC | |
| Status hukum | |
| Status hukum | |
| Data farmakokinetika | |
| Pengikatan protein | Mungkin tinggi[4] |
| Metabolisme | Oksidasi (CYP3A) |
| Waktu paruh eliminasi | 48 jam |
| Ekskresi | Feses (68%), urin (14%) |
| Pengenal | |
| |
| Nomor CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| Ligan PDB | |
| CompTox Dashboard (EPA) | |
| Data sifat kimia dan fisik | |
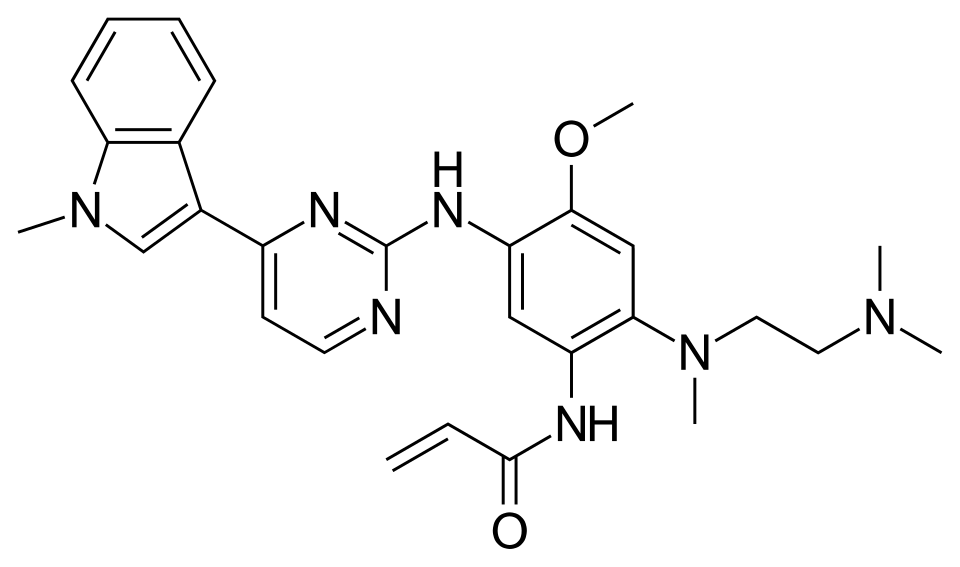
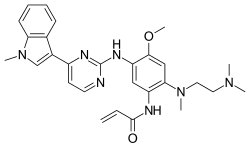
| Rumus | C28H33N7O2 |
| Massa molar | 499,62 g·mol−1 |
| Model 3D (JSmol) | |
| |
| |
Osimertinib[6] adalah obat yang digunakan untuk mengobati karsinoma paru non-sel kecil dengan mutasi spesifik.[7][8] Obat ini adalah penghambat tirosin kinase reseptor faktor pertumbuhan epidermal generasi ketiga.
Efek samping yang paling umum termasuk diare, ruam, nyeri muskuloskeletal, kulit kering, peradangan kulit di sekitar kuku, sakit mulut, kelelahan, dan batuk.[9]
Osimertinib disetujui untuk penggunaan medis di Amerika Serikat pada bulan November 2015,[10] dan di Uni Eropa pada bulan Februari 2016.[5]
Program penemuan obat yang menghasilkan osimertinib dimulai pada tahun 2009 dan menghasilkan obat ini pada tahun 2012; proses tersebut digerakkan oleh struktur dan bertujuan untuk menemukan penghambat EGFR generasi ketiga yang secara selektif akan menargetkan reseptor EGFR bentuk T790M.[11]
Osimertinib ditetapkan sebagai terapi terobosan pada bulan April 2014, berdasarkan hasil uji coba fase I,[11] dan obat ini disetujui sementara berdasarkan program persetujuan dipercepat FDA dengan voucher tinjauan prioritas pada bulan November 2015.[10][12]
Pada bulan Februari 2016, EMA menyetujui sementara osimertinib berdasarkan proses yang dipercepat—persetujuan pertama berdasarkan program tersebut.[5][11]
Pada bulan Februari 2024, FDA menyetujui osimertinib, dalam kombinasi dengan kemoterapi berbasis platinum, untuk orang dengan kanker paru-paru non-sel kecil lokal lanjut atau metastasis yang tumornya memiliki delesi EGFR ekson 19 atau mutasi ekson 21 L858R, seperti yang dideteksi oleh uji yang disetujui FDA. Khasiat dievaluasi dalam FLAURA 2 (NCT04035486), uji coba acak berlabel terbuka dari 557 peserta dengan delesi EGFR ekson 19 atau mutasi ekson 21 L858R positif la/mNSCLC dan tidak ada terapi sistemik sebelumnya untuk penyakit lanjut. Peserta diacak 1:1 untuk menerima osimertinib dengan kemoterapi berbasis platinum atau monoterapi osimertinib.[13] Aplikasi tersebut diberikan tinjauan prioritas, jalur cepat, terapi terobosan, dan penunjukan obat piatu.
Osimertinib digunakan untuk mengobati kanker paru-paru non-sel kecil (NSCLC) stadium lanjut atau metastasis, jika sel kanker positif mengalami mutasi T790M pada gen yang mengkode EGFR atau mengaktifkan mutasi EGFR.[4][14] Mutasi T790M dapat terjadi secara de novo atau didapat setelah pengobatan lini pertama dengan penghambat tirosin kinase EGFR lainnya seperti gefitinib, erlotinib, dan afatinib.[15]
Di AS, delesi ekson 19 EGFR, mutasi ekson 21 L858R, atau status T790M pasien sebelum pengobatan dengan osimertinib harus dideteksi melalui uji diagnostik pendamping.[4] Badan Pengawas Obat dan Makanan Amerika Serikat (FDA) telah menyetujui beberapa uji, termasuk FoundationOne CDx untuk tujuan ini.[16] Di Eropa dan tempat lain, aktivasi mutasi EGFR atau mutasi T790M dapat ditentukan dengan uji yang tervalidasi.[17]
Pada bulan Februari 2024, FDA menyetujui osimertinib, dalam kombinasi dengan kemoterapi berbasis platinum, untuk orang dengan kanker paru-paru non-sel kecil stadium lanjut atau metastasis yang tumornya memiliki delesi ekson 19 EGFR atau mutasi ekson 21 L858R, seperti yang dideteksi oleh uji yang disetujui FDA.[13]
Pada orang yang diobati dengan osimertinib, resistensi biasanya berkembang dalam waktu sekitar sepuluh bulan.[18] Resistensi yang dimediasi oleh mutasi ekson 20 C797S merupakan penyebab sebagian besar kasus resistensi,[19] yang mengakibatkan berbagai upaya dengan penghambat non-ATP kompetitif atau alosterik untuk mencoba dan mengimbangi resistensi yang didapat ini dengan menargetkan wilayah lain dari domain kinase RTK.[20]
Pada bulan September 2024, FDA menyetujui osimertinib untuk orang dewasa dengan kanker paru-paru non-sel kecil (NSCLC) stadium lanjut lokal yang tidak dapat direseksi (stadium III) yang penyakitnya tidak berkembang selama atau setelah terapi kemoradiasi berbasis platinum bersamaan atau berurutan, dan yang tumornya memiliki delesi ekson 19 EGFR atau mutasi ekson 21 L858R, seperti yang dideteksi oleh uji yang disetujui FDA.[21]
Efek samping yang sangat umum (lebih dari 10% subjek uji klinis) meliputi diare, stomatitis, ruam, kulit kering atau gatal, infeksi pada bagian jari tangan atau kaki yang bersentuhan dengan kulit, jumlah trombosit rendah, jumlah leukosit rendah, dan jumlah neutrofil rendah.[22]
Efek samping yang umum (antara 1% dan 10% subjek uji klinis) meliputi penyakit paru interstisial.[22]
Osimertinib dimetabolisme oleh CYP3A4 dan CYP3A5, sehingga zat yang sangat menghambat salah satu enzim, seperti antibiotik makrolida, antijamur, dan antivirus dapat meningkatkan paparan terhadap osimertinib, dan zat seperti rifampisin yang mengaktifkan salah satu enzim dapat menurunkan efektivitas osimertinib.[4][22]
Osimertinib lebih suka mengikat secara ireversibel pada protein reseptor faktor pertumbuhan epidermal yang bermutasi, terutama yang memiliki mutasi yang lebih umum pada kanker paru-paru seperti mutasi L858R atau penghapusan ekson 19.[4]
Osimertinib menunjukkan farmakokinetik linear; waktu rata-rata hingga Cmax adalah 6 jam (kisaran 3–24 jam). Estimasi waktu paruh rata-rata adalah 48 jam, dan klirens oral (CL/F) adalah 14,3 (L/jam). 68% eliminasi dilakukan melalui feses dan 14% melalui urin.[4]
Osimertinib tersedia sebagai mesilat; rumus kimianya adalah C28H33N7O2·CH4O3S, dan berat molekulnya adalah 596 g/mol. Nama kimianya adalah garam mesilat N-(2-{2-dimetilaminoetil-metilamino}-4-metoksi-5-{[4-(1-metilindol-3-il)pirimidin-2-il]amino}fenil)prop-2-enamida.[4]
Saat peluncurannya di Amerika Serikat, AstraZeneca mematok harganya sebesar US$12.750 per bulan.[24]: 59