Nanoteknologi DNA adalah perancangan dan pembuatan struktur asam nukleat buatan untuk keperluan teknologi. Dalam bidang ini, asam nukleat digunakan sebagai bahan rekayasa non-biologis bagi nanoteknologi, alih-alih sebagai pembawa informasi genetik dalam sel hidup. Para peneliti telah menciptakan struktur statis seperti kisi kristal dua dan tiga dimensi, nanotabung, polihedra, serta bentuk-bentuk arbitrer, juga perangkat fungsional seperti mesin molekuler dan komputer DNA. Bidang ini mulai dimanfaatkan sebagai perangkat untuk memecahkan persoalan ilmu dasar dalam biologi struktural dan biofisika, termasuk penerapan dalam kristalografi sinar-X dan spektroskopi resonansi magnet inti protein guna menentukan struktur. Aplikasi potensial dalam elektronika skala molekuler dan ilmu kedokteran nano juga tengah diteliti.
Sumber: Lihat artikel asli di Wikipedia


Nanoteknologi DNA adalah perancangan dan pembuatan struktur asam nukleat buatan untuk keperluan teknologi. Dalam bidang ini, asam nukleat digunakan sebagai bahan rekayasa non-biologis bagi nanoteknologi, alih-alih sebagai pembawa informasi genetik dalam sel hidup. Para peneliti telah menciptakan struktur statis seperti kisi kristal dua dan tiga dimensi, nanotabung, polihedra, serta bentuk-bentuk arbitrer, juga perangkat fungsional seperti mesin molekuler dan komputer DNA. Bidang ini mulai dimanfaatkan sebagai perangkat untuk memecahkan persoalan ilmu dasar dalam biologi struktural dan biofisika, termasuk penerapan dalam kristalografi sinar-X dan spektroskopi resonansi magnet inti protein guna menentukan struktur. Aplikasi potensial dalam elektronika skala molekuler dan ilmu kedokteran nano juga tengah diteliti.
Landasan konseptual nanoteknologi DNA pertama kali dirumuskan oleh Nadrian Seeman pada awal dekade 1980-an, dan bidang ini mulai menarik perhatian luas pada pertengahan tahun 2000-an. Pemanfaatan asam nukleat ini dimungkinkan oleh kaidah pemasangan pasangan basa yang ketat, yang menyebabkan hanya bagian-bagian untai dengan komplementaritas urutan basa yang dapat saling berikatan membentuk struktur heliks ganda asam nukleat yang kuat dan kaku. Hal ini memungkinkan perancangan rasional urutan basa yang akan merakit dirinya secara selektif untuk membentuk struktur target yang kompleks dengan fitur nanoskala yang terkontrol secara presisi. Beragam metode perakitan digunakan untuk menghasilkan struktur-struktur tersebut, termasuk struktur berbasis ubin yang tersusun dari unit-unit kecil, struktur lipatan menggunakan metode origami DNA, serta struktur yang dapat dikonfigurasi ulang secara dinamis melalui metode perpindahan untai. Penamaan bidang ini secara khusus merujuk pada DNA, namun prinsip yang sama juga diterapkan pada jenis asam nukleat lainnya, sehingga terkadang digunakan sebutan alternatif nanoteknologi asam nukleat.
Landasan konseptual nanoteknologi DNA pertama kali dirumuskan oleh Nadrian Seeman pada awal 1980-an.[2] Motivasi awal Seeman adalah menciptakan kisi DNA tiga dimensi untuk mengorientasikan molekul besar lainnya, yang akan menyederhanakan studi kristalografi molekul tersebut dengan menghilangkan proses sulit untuk mendapatkan kristal murni. Ide ini kabarnya muncul padanya pada akhir tahun 1980, setelah menyadari kemiripan antara karya cukil kayu Depth oleh M. C. Escher dan susunan persimpangan enam lengan DNA.[3][4] Beberapa struktur DNA bercabang alami telah diketahui pada saat itu, termasuk garpu replikasi DNA dan persimpangan Holliday yang bergerak, namun pemikiran Seeman adalah bahwa persimpangan asam nukleat yang imobil dapat diciptakan dengan merancang urutan untai secara tepat untuk menghilangkan simetri pada molekul yang dirakit, dan bahwa persimpangan imobil ini pada prinsipnya dapat digabungkan menjadi kisi kristal yang kaku. Makalah teoretis pertama yang mengusulkan skema ini diterbitkan pada tahun 1982, dan demonstrasi eksperimental pertama dari persimpangan DNA imobil diterbitkan pada tahun berikutnya.[5][6]
Pada tahun 1991, laboratorium Seeman menerbitkan laporan tentang sintesis kubus yang terbuat dari DNA, nanostruktur asam nukleat tiga dimensi sintetik pertama, yang karenanya ia menerima Hadiah Feynman dalam Nanoteknologi tahun 1995. Penemuan ini diikuti oleh oktahedron terpotong DNA. Segera menjadi jelas bahwa struktur-struktur ini, bentuk-bentuk poligonal dengan persimpangan fleksibel sebagai titik sudutnya, tidak cukup kaku untuk membentuk kisi tiga dimensi yang diperluas. Seeman mengembangkan motif struktural pindah silang ganda (DX) yang lebih kaku, dan pada tahun 1998, bekerja sama dengan Erik Winfree, mempublikasikan penciptaan kisi dua dimensi dari ubin DX.[3][2][7] Struktur berbasis ubin ini memiliki keunggulan karena menyediakan kemampuan untuk mengimplementasikan komputasi DNA, yang didemonstrasikan oleh Winfree dan Paul Rothemund dalam makalah tahun 2004 mereka mengenai perakitan mandiri algoritmik struktur paking Sierpinski, dan karenanya mereka berbagi Hadiah Feynman dalam Nanoteknologi tahun 2006. Wawasan kunci Winfree adalah bahwa ubin DX dapat digunakan sebagai ubin Wang, yang berarti perakitannya dapat melakukan komputasi.[2] Sintesis kisi tiga dimensi akhirnya dipublikasikan oleh Seeman pada tahun 2009, hampir tiga puluh tahun setelah ia mulai berupaya mencapainya.[8]
Kemampuan-kemampuan baru terus ditemukan untuk struktur DNA yang dirancang sepanjang tahun 2000-an. Nanomesin DNA pertama—sebuah motif yang mengubah strukturnya sebagai respons terhadap masukan—didemonstrasikan pada tahun 1999 oleh Seeman. Sistem yang lebih baik, yang merupakan perangkat asam nukleat pertama yang memanfaatkan pemindahan untai yang dimediasi tumpuan (toehold), didemonstrasikan oleh Bernard Yurke pada tahun 2000.[9] Kemajuan berikutnya adalah menerjemahkan ini menjadi gerakan mekanis, dan pada tahun 2004 serta 2005, beberapa sistem pejalan DNA didemonstrasikan oleh kelompok riset Seeman, Niles Pierce, Andrew Turberfield, dan Chengde Mao.[10] Gagasan penggunaan larik DNA untuk menjadi templat perakitan molekul lain seperti nanopartikel dan protein, yang pertama kali disarankan oleh Bruche Robinson dan Seeman pada tahun 1987,[11] didemonstrasikan pada tahun 2002 oleh Seeman, Kiehl dkk.[12] dan selanjutnya oleh banyak kelompok lain.
Pada tahun 2006, Rothemund pertama kali mendemonstrasikan metode origami DNA untuk membentuk struktur DNA terlipat dengan bentuk sembarang secara mudah dan kuat. Rothemund telah menyusun metode ini sebagai perantara konseptual antara kisi DX Seeman, yang menggunakan banyak untai pendek, dan oktahedron DNA karya William Shih, yang sebagian besar terdiri dari satu untai yang sangat panjang. Origami DNA Rothemund berisi satu untai panjang yang pelipatannya dibantu oleh beberapa untai pendek. Metode ini memungkinkan pembentukan struktur yang jauh lebih besar daripada yang sebelumnya dimungkinkan, serta tidak terlalu menuntut secara teknis untuk dirancang dan disintesis.[7] Origami DNA menjadi berita sampul jurnal Nature pada 15 Maret 2006.[13] Penelitian Rothemund yang mendemonstrasikan struktur origami DNA dua dimensi diikuti oleh demonstrasi origami DNA tiga dimensi padat oleh Douglas dkk. pada tahun 2009,[14] sementara laboratorium Jørgen Kjems dan Yan mendemonstrasikan struktur tiga dimensi berongga yang terbuat dari sisi-sisi dua dimensi.[8]
Nanoteknologi DNA awalnya ditanggapi dengan skeptisisme karena penggunaan nonbiologis asam nukleat yang tidak lazim sebagai bahan untuk membangun struktur dan melakukan komputasi, serta banyaknya eksperimen bukti prinsip yang memperluas kemampuan bidang ini namun masih jauh dari aplikasi nyata. Makalah Seeman tahun 1991 tentang sintesis kubus DNA ditolak oleh jurnal Science setelah satu peninjau memuji orisinalitasnya sementara yang lain mengkritiknya karena kurangnya relevansi biologis.[15] Pada awal 2010-an, bidang ini dianggap telah meningkatkan kemampuannya hingga pada titik di mana aplikasi untuk penelitian ilmu dasar mulai terwujud, dan aplikasi praktis dalam kedokteran serta bidang lainnya mulai dianggap layak.[8][16] Bidang ini telah berkembang dari sangat sedikit laboratorium aktif pada tahun 2001 menjadi setidaknya 60 pada tahun 2010, yang meningkatkan kumpulan bakat dan dengan demikian jumlah kemajuan ilmiah di bidang tersebut selama dekade itu.[17]

Nanoteknologi sering didefinisikan sebagai studi tentang material dan perangkat dengan fitur pada skala di bawah 100 nanometer. Nanoteknologi DNA, secara khusus, adalah contoh dari bawah-ke-atas perakitan mandiri molekuler, di mana komponen molekuler secara spontan mengatur diri menjadi struktur yang stabil; bentuk khusus dari struktur ini diinduksi oleh sifat fisik dan kimia dari komponen yang dipilih oleh para perancang.[19] Dalam nanoteknologi DNA, material komponennya adalah untai asam nukleat seperti DNA; untai ini seringkali sintetik dan hampir selalu digunakan di luar konteks sel hidup. DNA sangat cocok untuk konstruksi skala nano karena ikatan antara dua untai asam nukleat bergantung pada aturan pasangan basa sederhana yang dipahami dengan baik, dan membentuk struktur skala nano spesifik dari heliks ganda asam nukleat. Kualitas ini membuat perakitan struktur asam nukleat mudah dikendalikan melalui desain asam nukleat. Sifat ini tidak dimiliki oleh material lain yang digunakan dalam nanoteknologi, termasuk protein, yang desain proteinnya sangat sulit, dan nanopartikel, yang tidak memiliki kemampuan untuk melakukan perakitan spesifik secara mandiri.[5]
Struktur molekul asam nukleat terdiri dari urutan nukleotida yang dibedakan berdasarkan nukleobasa yang dikandungnya. Dalam DNA, empat basa yang ada adalah adenina (A), sitosina (C), guanina (G), dan timina (T). Asam nukleat memiliki sifat bahwa dua molekul hanya akan berikatan satu sama lain untuk membentuk heliks ganda jika kedua urutan tersebut komplementer, yang berarti mereka membentuk urutan pasangan basa yang cocok, dengan A hanya berikatan dengan T, dan C hanya dengan G.[5][20] Karena pembentukan pasangan basa yang cocok secara tepat itu menguntungkan secara energetik, untai asam nukleat pada sebagian besar kasus diharapkan akan berikatan satu sama lain dalam konformasi yang memaksimalkan jumlah basa yang berpasangan secara benar. Dengan demikian, urutan basa dalam sistem untai menentukan pola pengikatan dan struktur keseluruhan dengan cara yang mudah dikendalikan. Dalam nanoteknologi DNA, urutan basa untai dirancang secara rasional oleh para peneliti sehingga interaksi pasangan basa menyebabkan untai merakit diri dalam konformasi yang diinginkan.[3][5] Meskipun DNA adalah material dominan yang digunakan, struktur yang menggabungkan asam nukleat lain seperti RNA dan asam nukleat peptida (PNA) juga telah dikonstruksi.[21][22]
Nanoteknologi DNA terkadang dibagi menjadi dua subbidang yang saling tumpang tindih: nanoteknologi DNA struktural dan nanoteknologi DNA dinamis. Nanoteknologi DNA struktural, terkadang disingkat SDN, berfokus pada menyintesis dan mengarakterisasi kompleks asam nukleat dan material yang merakit diri menjadi keadaan akhir keseimbangan statis. Di sisi lain, nanoteknologi DNA dinamis berfokus pada kompleks dengan perilaku non-keseimbangan yang berguna seperti kemampuan untuk mengonfigurasi ulang berdasarkan stimulus kimia atau fisik. Beberapa kompleks, seperti perangkat nanomekanis asam nukleat, menggabungkan fitur dari kedua subbidang struktural dan dinamis.[23][24]
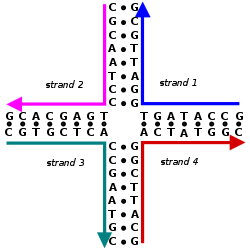
Kompleks yang dikonstruksi dalam nanoteknologi DNA struktural menggunakan struktur asam nukleat yang bercabang secara topologis dan mengandung persimpangan. (Sebaliknya, sebagian besar DNA biologis ada sebagai heliks ganda tak bercabang.) Salah satu struktur bercabang yang paling sederhana adalah persimpangan empat lengan yang terdiri dari empat untai DNA individu, yang sebagian darinya saling komplementer dalam pola tertentu. Tidak seperti pada persimpangan Holliday alami, setiap lengan pada persimpangan empat lengan imobil buatan memiliki urutan basa yang berbeda, menyebabkan titik persimpangan terpaku pada posisi tertentu. Beberapa persimpangan dapat digabungkan dalam kompleks yang sama, seperti pada motif struktural pindah silang ganda (DX) yang digunakan secara luas, yang mengandung dua domain heliks ganda paralel dengan untai individu yang melintas di antara domain pada dua titik pindah silang. Setiap titik pindah silang, secara topologis, adalah persimpangan empat lengan, namun dibatasi pada satu orientasi, berbeda dengan persimpangan empat lengan tunggal yang fleksibel, memberikan kekakuan yang membuat motif DX cocok sebagai blok bangunan struktural untuk kompleks DNA yang lebih besar.[3][5]
Nanoteknologi DNA dinamis menggunakan mekanisme yang disebut pemindahan untai yang dimediasi tumpuan (toehold) untuk memungkinkan kompleks asam nukleat mengonfigurasi ulang sebagai respons terhadap penambahan untai asam nukleat baru. Dalam reaksi ini, untai yang masuk berikatan dengan wilayah tumpuan untai tunggal dari kompleks untai ganda, dan kemudian memindahkan salah satu untai yang terikat dalam kompleks asli melalui proses migrasi cabang. Efek keseluruhannya adalah salah satu untai dalam kompleks digantikan dengan untai lain.[23] Selain itu, struktur dan perangkat yang dapat dikonfigurasi ulang dapat dibuat menggunakan asam nukleat fungsional seperti deoksiribozim dan ribozim, yang dapat melakukan reaksi kimia, serta aptamer, yang dapat berikatan dengan protein atau molekul kecil tertentu.[25]
Nanoteknologi DNA struktural, terkadang disingkat SDN, berfokus pada menyintesis dan mengarakterisasi kompleks asam nukleat dan material di mana perakitannya memiliki titik akhir keseimbangan statis. Heliks ganda asam nukleat memiliki geometri tiga dimensi yang kokoh dan terdefinisi yang memungkinkan untuk mensimulasikan,[26] memprediksi, dan merancang struktur kompleks asam nukleat yang lebih rumit. Banyak struktur seperti itu telah diciptakan, termasuk struktur dua dan tiga dimensi, serta struktur periodik, aperiodik, dan diskret.[24]

Kompleks asam nukleat kecil dapat dilengkapi dengan ujung lengket dan digabungkan menjadi kisi periodik dua dimensi yang lebih besar yang mengandung pola teselasi spesifik dari ubin molekuler individu.[24] Contoh paling awal dari hal ini menggunakan kompleks pindah silang ganda (DX) sebagai ubin dasar, yang masing-masing mengandung empat ujung lengket yang dirancang dengan urutan yang menyebabkan unit DX bergabung menjadi lembaran datar dua dimensi periodik yang pada dasarnya merupakan kristal DNA dua dimensi yang kaku.[30][31] Larik dua dimensi juga telah dibuat dari motif lain, termasuk kisi belah ketupat persimpangan Holliday,[32] dan berbagai larik berbasis DX yang memanfaatkan skema kohesi ganda.[33][34] Dua gambar teratas di sebelah kanan menunjukkan contoh kisi periodik berbasis ubin.
Larik dua dimensi dapat dibuat untuk menunjukkan struktur aperiodik yang perakitannya mengimplementasikan algoritme tertentu, yang menunjukkan salah satu bentuk komputasi DNA.[17] Ubin DX dapat dipilih urutan ujung lengketnya sehingga bertindak sebagai ubin Wang, yang memungkinkannya melakukan komputasi. Sebuah larik DX yang perakitannya menyandikan operasi XOR telah didemonstrasikan; hal ini memungkinkan larik DNA tersebut mengimplementasikan otomata seluler yang menghasilkan fraktal yang dikenal sebagai paking Sierpinski. Gambar ketiga di sebelah kanan menunjukkan jenis larik ini.[29] Sistem lain memiliki fungsi sebagai pencacah biner, yang menampilkan representasi angka biner yang meningkat seiring pertumbuhannya. Hasil-hasil ini menunjukkan bahwa komputasi dapat dimasukkan ke dalam perakitan larik DNA.[35]
Larik DX telah dibuat untuk membentuk nanotabung berongga berdiameter 4–20 nm, yang pada dasarnya merupakan kisi dua dimensi yang melengkung kembali ke dirinya sendiri.[36] Nanotabung DNA ini agak mirip dalam ukuran dan bentuk dengan nanotabung karbon, dan meskipun tidak memiliki konduktansi listrik seperti nanotabung karbon, nanotabung DNA lebih mudah dimodifikasi dan dihubungkan ke struktur lain. Salah satu dari banyak skema untuk mengonstruksi nanotabung DNA menggunakan kisi ubin DX melengkung yang menggulung dirinya sendiri dan menutup menjadi tabung.[37] Dalam metode alternatif yang memungkinkan keliling tabung ditentukan dengan cara modular yang sederhana menggunakan ubin untai tunggal, kekakuan tabung tersebut adalah sifat emergen.[38]
Membentuk kisi DNA tiga dimensi adalah tujuan paling awal dari nanoteknologi DNA, namun hal ini terbukti menjadi salah satu yang paling sulit untuk direalisasikan. Keberhasilan menggunakan motif berdasarkan konsep tensegritas, keseimbangan antara gaya tarik dan tekan, akhirnya dilaporkan pada tahun 2009.[17][39]
Para peneliti telah menyintesis banyak kompleks DNA tiga dimensi yang masing-masing memiliki konektivitas poliedron, seperti kubus atau oktahedron, yang berarti bahwa dupleks DNA menelusuri rusuk poliedron dengan persimpangan DNA di setiap titik sudut.[6] Demonstrasi paling awal dari poliedra DNA sangatlah padat karya, membutuhkan beberapa langkah ligasi dan sintesis fase padat untuk menciptakan poliedra terkatenasi.[40] Penelitian selanjutnya menghasilkan poliedra yang sintesisnya jauh lebih mudah. Ini termasuk oktahedron DNA yang terbuat dari untai tunggal panjang yang dirancang untuk melipat menjadi konformasi yang benar,[41] serta tetrahedron yang dapat diproduksi dari empat untai DNA dalam satu langkah, sebagaimana digambarkan di bagian atas artikel ini.[1]
Nanostruktur dengan bentuk sembarang dan tak beraturan biasanya dibuat menggunakan metode origami DNA. Struktur-struktur ini terdiri dari untai virus alami yang panjang sebagai "perancah", yang dibuat melipat menjadi bentuk yang diinginkan dengan bantuan untai "stapel" pendek yang dirancang secara komputasional. Metode ini memiliki keunggulan berupa kemudahan desain, karena urutan basanya telah ditentukan sebelumnya oleh urutan untai perancah, serta tidak memerlukan kemurnian untai yang tinggi dan stoikiometri yang akurat, sebagaimana dibutuhkan oleh sebagian besar metode nanoteknologi DNA lainnya. Origami DNA pertama kali didemonstrasikan untuk bentuk-bentuk dua dimensi, seperti wajah tersenyum, peta kasar Belahan Bumi Barat, dan lukisan Mona Lisa.[6][13][42] Struktur tiga dimensi padat dapat dibuat dengan menggunakan heliks DNA paralel yang disusun dalam pola sarang lebah,[14] dan struktur dengan sisi-sisi dua dimensi dapat dibuat melipat menjadi bentuk tiga dimensi keseluruhan yang berongga, mirip dengan kotak kardus. Struktur ini dapat diprogram untuk membuka dan menyingkap atau melepaskan muatan molekuler sebagai respons terhadap stimulus, menjadikannya berpotensi berguna sebagai sangkar molekuler yang dapat diprogram.[43][44]
Struktur asam nukleat dapat dibuat untuk menggabungkan molekul selain asam nukleat, terkadang disebut heteroelemen, termasuk protein, nanopartikel logam, titik kuantum, amina,[45] dan fulerena. Hal ini memungkinkan konstruksi material dan perangkat dengan rentang fungsionalitas yang jauh lebih besar daripada yang dimungkinkan dengan asam nukleat saja. Tujuannya adalah menggunakan perakitan mandiri struktur asam nukleat untuk menjadi templat bagi perakitan nanopartikel yang ditampung di atasnya, serta mengendalikan posisi dan dalam beberapa kasus orientasinya.[6][46] Banyak dari skema ini menggunakan metode pengikatan kovalen, menggunakan oligonukleotida dengan gugus fungsi amida atau tiol sebagai pegangan kimia untuk mengikat heteroelemen tersebut. Skema pengikatan kovalen ini telah digunakan untuk mengatur nanopartikel emas pada larik berbasis DX,[47] dan untuk mengatur molekul protein streptavidin ke dalam pola spesifik pada larik DX.[48] Skema penampungan nonkovalen menggunakan poliamida Dervan pada larik DX digunakan untuk mengatur protein streptavidin dalam pola spesifik pada larik DX.[49] Nanotabung karbon telah ditampung pada larik DNA dalam pola yang memungkinkan perakitan tersebut bertindak sebagai perangkat elektronik molekuler, sebuah transistor efek medan nanotabung karbon.[50] Selain itu, terdapat metode metalisasi asam nukleat, di mana asam nukleat digantikan oleh logam yang mengambil bentuk umum struktur asam nukleat aslinya,[51] dan skema untuk menggunakan nanostruktur asam nukleat sebagai masker litografi, yang mentransfer polanya ke permukaan padat.[52]

Nanoteknologi DNA dinamis berfokus pada pembentukan sistem asam nukleat dengan fungsionalitas dinamis yang dirancang terkait dengan struktur keseluruhannya, seperti komputasi dan gerakan mekanis. Terdapat beberapa tumpang tindih antara nanoteknologi DNA struktural dan dinamis, karena struktur dapat dibentuk melalui proses anil dan kemudian dikonfigurasi ulang secara dinamis, atau dapat dibuat untuk terbentuk secara dinamis sejak awal.[6][10]
Telah dibuat kompleks DNA yang mengubah konformasinya ketika diberi stimulus tertentu, menjadikannya salah satu bentuk nanorobotika. Struktur ini awalnya dibentuk dengan cara yang sama seperti struktur statis yang dibuat dalam nanoteknologi DNA struktural, tetapi dirancang agar konfigurasi ulang dinamis dimungkinkan setelah perakitan awal.[23][10] Perangkat paling awal semacam ini memanfaatkan transisi antara bentuk B-DNA dan Z-DNA untuk merespons perubahan kondisi penyangga dengan melakukan gerakan memuntir.[53] Ketergantungan pada kondisi penyangga ini menyebabkan semua perangkat berubah keadaan pada saat yang bersamaan. Sistem-sistem selanjutnya dapat mengubah keadaan berdasarkan keberadaan untai kendali, yang memungkinkan beberapa perangkat dioperasikan secara independen dalam larutan. Beberapa contoh sistem tersebut adalah desain "pinset molekuler" yang memiliki keadaan terbuka dan tertutup,[54] perangkat yang dapat beralih dari konformasi pindah silang paranemik (PX) ke konformasi (JX2) dengan dua jukstaposisi tulang punggung DNA tanpa persimpangan, yang mengalami gerakan rotasi dalam prosesnya,[55] dan larik dua dimensi yang dapat memuai dan menyusut secara dinamis sebagai respons terhadap untai kendali.[56] Struktur juga telah dibuat agar dapat membuka atau menutup secara dinamis, yang berpotensi bertindak sebagai sangkar molekuler untuk melepaskan atau menyingkap muatan fungsional saat dibuka.[43][57][58] Dalam contoh lain, nanostruktur origami DNA dipasangkan dengan RNA polimerase T7 dan dengan demikian dapat dioperasikan sebagai motor bertenaga energi kimia yang dapat dipasangkan dengan pengikut pasif, yang kemudian digerakkannya.[59]
Pejalan DNA adalah kelas nanomesin asam nukleat yang menunjukkan gerakan terarah di sepanjang lintasan linear. Sejumlah besar skema telah didemonstrasikan.[10] Salah satu strateginya adalah mengendalikan gerakan pejalan di sepanjang lintasan menggunakan untai kendali yang perlu ditambahkan secara manual secara berurutan.[60][61] Dimungkinkan juga untuk mengendalikan langkah individu pejalan DNA melalui penyinaran dengan cahaya yang memiliki panjang gelombang berbeda.[62] Pendekatan lain adalah memanfaatkan enzim restriksi atau deoksiribozim untuk memotong untai dan menyebabkan pejalan bergerak maju, yang memiliki keunggulan dapat berjalan secara otonom.[63][64] Sistem yang lebih baru dapat berjalan di atas permukaan dua dimensi alih-alih lintasan linear, dan mendemonstrasikan kemampuan untuk mengambil dan memindahkan muatan molekuler secara selektif.[65] Pada tahun 2018, sebuah DNA terkatenasi yang menggunakan transkripsi lingkaran bergulir oleh RNA polimerase T7 yang terpasang terbukti berjalan di sepanjang jalur DNA, dipandu oleh untai RNA yang dihasilkan.[66] Selain itu, pejalan linear telah didemonstrasikan melakukan sintesis bertemplat DNA saat pejalan bergerak maju di sepanjang lintasan, memungkinkan sintesis kimia bertahap otonom yang diarahkan oleh pejalan tersebut.[67] Fungsi pejalan DNA sintetik ini mirip dengan fungsi protein dinein dan kinesin.[68]
Kaskade reaksi pemindahan untai dapat digunakan baik untuk tujuan komputasional maupun struktural. Sebuah reaksi pemindahan untai tunggal melibatkan penyingkapan urutan baru sebagai respons terhadap keberadaan suatu untai inisiator. Banyak reaksi semacam itu dapat dihubungkan menjadi sebuah kaskade di mana urutan keluaran yang baru terungkap dari satu reaksi dapat memicu reaksi pemindahan untai lainnya di tempat lain. Hal ini pada gilirannya memungkinkan konstruksi jejaring reaksi kimia dengan banyak komponen, yang menunjukkan kemampuan komputasi dan pemrosesan informasi yang kompleks. Kaskade ini dibuat menguntungkan secara energetik melalui pembentukan pasangan basa baru, dan perolehan entropi dari reaksi penguraian. Kaskade pemindahan untai memungkinkan operasi isotermal dari proses perakitan atau komputasi tersebut, berbeda dengan perakitan asam nukleat tradisional yang mensyaratkan langkah anil termal, di mana suhu dinaikkan dan kemudian diturunkan secara perlahan untuk memastikan pembentukan struktur yang diinginkan secara tepat. Kaskade ini juga dapat mendukung fungsi katalitik dari spesies inisiator, di mana kurang dari satu ekuivalen inisiator dapat menyebabkan reaksi berjalan hingga selesai.[23][69]
Kompleks pemindahan untai dapat digunakan untuk membuat gerbang logika molekuler yang mampu melakukan komputasi kompleks.[70] Tidak seperti komputer elektronik tradisional, yang menggunakan arus listrik sebagai masukan dan keluaran, komputer molekuler menggunakan konsentrasi spesies kimia tertentu sebagai sinyal. Dalam kasus sirkuit pemindahan untai asam nukleat, sinyalnya adalah keberadaan untai asam nukleat yang dilepaskan atau dikonsumsi oleh peristiwa pengikatan dan pelepasan ikatan pada untai lain dalam kompleks pemindahan. Pendekatan ini telah digunakan untuk membuat gerbang logika seperti gerbang AND, OR, dan NOT.[71] Baru-baru ini, sebuah sirkuit empat bit didemonstrasikan dapat menghitung akar kuadrat dari bilangan bulat 0–15, menggunakan sistem gerbang yang berisi 130 untai DNA.[72]
Kegunaan lain dari kaskade pemindahan untai adalah untuk membuat struktur yang dirakit secara dinamis. Metode ini menggunakan struktur jepit rambut untuk reaktan, sehingga ketika untai masukan berikatan, urutan yang baru terungkap berada pada molekul yang sama alih-alih terurai. Hal ini memungkinkan jepit rambut yang baru terbuka untuk ditambahkan ke kompleks yang sedang tumbuh. Pendekatan ini telah digunakan untuk membuat struktur sederhana seperti persimpangan tiga dan empat lengan serta dendrimer.[69]
Nanoteknologi DNA menyediakan salah satu dari sedikit cara untuk membentuk struktur yang kompleks dan dirancang dengan kendali presisi atas fitur skala nano. Bidang ini mulai melihat penerapan untuk memecahkan masalah ilmu dasar dalam biologi struktural dan biofisika. Aplikasi paling awal yang dibayangkan untuk bidang ini, dan yang masih dalam pengembangan, adalah dalam kristalografi, di mana molekul yang sulit dikristalisasi secara terisolasi dapat diatur di dalam kisi asam nukleat tiga dimensi, yang memungkinkan penentuan strukturnya. Aplikasi lainnya adalah penggunaan batang origami DNA untuk menggantikan kristal cair dalam eksperimen kopling dipolar residual pada spektroskopi NMR protein; penggunaan origami DNA menguntungkan karena, tidak seperti kristal cair, origami DNA toleran terhadap deterjen yang dibutuhkan untuk mensuspensi protein membran dalam larutan. Pejalan DNA telah digunakan sebagai jalur perakitan skala nano untuk memindahkan nanopartikel dan mengarahkan sintesis kimia. Lebih jauh lagi, struktur origami DNA telah membantu dalam studi biofisika mengenai fungsi enzim dan pelipatan protein.[24][8]
Nanoteknologi DNA bergerak menuju aplikasi dunia nyata yang potensial. Kemampuan larik asam nukleat untuk mengatur molekul lain menunjukkan potensi aplikasinya dalam elektronika skala molekuler. Perakitan struktur asam nukleat dapat digunakan untuk menjadi templat bagi perakitan elemen elektronik molekuler seperti kawat molekuler, menyediakan metode untuk pengendalian skala nanometer atas penempatan dan arsitektur keseluruhan perangkat yang dianalogikan dengan papan sirkuit percobaan (breadboard) molekuler.[24][6] Nanoteknologi DNA telah dibandingkan dengan konsep materi terprogram karena penggabungan komputasi dengan sifat materialnya.[73]
Dalam sebuah studi yang dilakukan oleh sekelompok ilmuwan dari iNANO dan pusat CDNA di Universitas Aarhus, para peneliti mampu mengonstruksi Origami Kotak DNA 3D kecil yang dapat dialihkan secara ganda (multi-switchable). Nanopartikel yang diusulkan tersebut dikarakterisasi dengan mikroskopi gaya atom (AFM), mikroskopi elektron transmisi (TEM), dan transfer energi resonansi Förster (FRET). Kotak yang dikonstruksi terbukti memiliki mekanisme penutupan kembali yang unik, yang memungkinkannya untuk membuka dan menutup berulang kali sebagai respons terhadap satu set kunci DNA atau RNA yang unik. Para penulis mengusulkan bahwa "perangkat DNA ini berpotensi digunakan untuk berbagai aplikasi seperti mengendalikan fungsi molekul tunggal, penghantaran obat terkendali, dan komputasi molekuler."[74]
Terdapat potensi aplikasi untuk nanoteknologi DNA dalam nanomedis, yang memanfaatkan kemampuannya untuk melakukan komputasi dalam format yang biokompatibel untuk membuat "obat pintar" bagi penghantaran obat tertarget, serta untuk aplikasi diagnostik. Salah satu sistem yang sedang diselidiki menggunakan kotak DNA berongga yang berisi protein yang menginduksi apoptosis, atau kematian sel, yang hanya akan terbuka ketika berada di dekat sel kanker.[8][75] Selain itu, terdapat minat untuk mengekspresikan struktur buatan ini di dalam sel bakteri hidup yang direkayasa, kemungkinan besar menggunakan RNA yang ditranskripsikan untuk perakitannya, meskipun belum diketahui apakah struktur kompleks ini mampu melipat atau merakit secara efisien di dalam sitoplasma sel. Jika berhasil, hal ini dapat memungkinkan evolusi terarah dari nanostruktur asam nukleat.[6] Ilmuwan di Universitas Oxford melaporkan perakitan mandiri empat untai pendek DNA sintetik menjadi sebuah sangkar yang dapat memasuki sel dan bertahan setidaknya selama 48 jam. Tetrahedron DNA yang berlabel fluoresen ditemukan tetap utuh di dalam sel ginjal manusia yang dikultur di laboratorium meskipun terdapat serangan oleh enzim seluler setelah dua hari. Eksperimen ini menunjukkan potensi penghantaran obat di dalam sel hidup menggunakan 'sangkar' DNA.[76][77] Sebuah tetrahedron DNA digunakan untuk menghantarkan Interferensi RNA (RNAi) dalam model tikus, sebagaimana dilaporkan oleh tim peneliti di MIT. Penghantaran RNA penginterferensi untuk pengobatan telah menunjukkan keberhasilan menggunakan polimer atau lipid, namun terdapat batasan keamanan dan penargetan yang tidak tepat, di samping umur simpan yang pendek dalam aliran darah. Nanostruktur DNA yang dibuat oleh tim tersebut terdiri dari enam untai DNA untuk membentuk tetrahedron, dengan satu untai RNA ditempelkan pada masing-masing dari keenam tepinya. Tetrahedron tersebut selanjutnya dilengkapi dengan protein penargetan, tiga molekul folat, yang menuntun nanopartikel DNA ke reseptor folat melimpah yang ditemukan pada beberapa tumor. Hasilnya menunjukkan bahwa ekspresi gen yang ditargetkan oleh RNAi, lusiferase, turun lebih dari separuh. Studi ini menunjukkan harapan dalam penggunaan nanoteknologi DNA sebagai alat yang efektif untuk menghantarkan pengobatan menggunakan teknologi Interferensi RNA yang sedang berkembang.[78][79] Tetrahedron DNA juga digunakan dalam upaya untuk mengatasi fenomena resistansi multidobat. Doksorubisin (DOX) dikonjugasikan dengan tetrahedron dan dimuat ke dalam sel kanker payudara MCF-7 yang mengandung pompa efluks obat P-glikoprotein. Hasil eksperimen menunjukkan DOX tidak dipompa keluar dan apoptosis sel kanker tercapai. Tetrahedron tanpa DOX dimuat ke dalam sel untuk menguji biokompatibilitasnya, dan struktur tersebut tidak menunjukkan sitotoksisitas.[80] Tetrahedron DNA juga digunakan sebagai kode batang untuk membuat profil ekspresi dan distribusi subseluler protein dalam sel untuk tujuan diagnostik. Nanostruktur tetrahedral menunjukkan sinyal yang ditingkatkan karena efisiensi pelabelan dan stabilitas yang lebih tinggi.[81]
Aplikasi nanoteknologi DNA dalam nanomedis juga berfokus pada peniruan struktur dan fungsi protein membran yang terjadi secara alami dengan nanostruktur DNA yang dirancang. Pada tahun 2012, Langecker dkk.[82] memperkenalkan struktur origami DNA berbentuk pori yang dapat menyisip secara mandiri ke dalam membran lipid melalui modifikasi kolesterol hidrofobik dan menginduksi arus ionik melintasi membran. Demonstrasi pertama saluran ion DNA sintetik ini diikuti oleh berbagai desain penginduksi pori mulai dari dupleks DNA tunggal,[83] hingga struktur berbasis ubin kecil,[84][85][86][87][88] dan porin transmembran origami DNA besar.[89] Mirip dengan saluran ion protein yang terjadi secara alami, ansambel pasangan buatan DNA sintetik ini dengan demikian mencakup rentang konduktansi beberapa orde besaran. Studi tentang dupleks DNA tunggal yang menyisip ke membran menunjukkan bahwa arus juga harus mengalir pada antarmuka DNA-lipid karena tidak ada lumen saluran pusat dalam desain tersebut yang membiarkan ion melintas di lapis ganda lipid. Hal ini menunjukkan bahwa pori lipid yang diinduksi DNA memiliki bentuk toroidal, bukannya silinder, karena gugus kepala lipid berorientasi ulang menghadap ke arah bagian DNA yang tersisip di membran.[83] Para peneliti dari Universitas Cambridge dan Universitas Illinois Urbana-Champaign kemudian mendemonstrasikan bahwa pori toroidal yang diinduksi DNA semacam itu dapat memfasilitasi flip-flop lipid yang cepat di antara lembaran lapis ganda lipid. Dengan memanfaatkan efek ini, mereka merancang enzim buatan DNA sintetik yang membalik lipid dalam membran biologis beberapa orde besaran lebih cepat daripada protein alami yang disebut skramblase.[90] Pengembangan ini menyoroti potensi nanostruktur DNA sintetik untuk obat-obatan dan terapi yang dipersonalisasi.
Nanostruktur DNA harus dirancang secara rasional agar untai asam nukleat individu dapat merakit diri menjadi struktur yang diinginkan. Proses ini biasanya dimulai dengan spesifikasi struktur target atau fungsi yang diinginkan. Kemudian, struktur sekunder keseluruhan dari kompleks target ditentukan, yang menentukan susunan untai asam nukleat di dalam struktur tersebut, serta bagian mana dari untai-untai tersebut yang harus berikatan satu sama lain. Langkah terakhir adalah desain struktur primer, yaitu spesifikasi urutan basa aktual dari setiap untai asam nukleat.[36][91]
Langkah pertama dalam merancang nanostruktur asam nukleat adalah memutuskan bagaimana struktur tertentu harus direpresentasikan oleh susunan spesifik untai asam nukleat. Langkah desain ini menentukan struktur sekunder, atau posisi pasangan basa yang menyatukan untai-untai individu dalam bentuk yang diinginkan.[36] Beberapa pendekatan telah didemonstrasikan:
Setelah salah satu pendekatan di atas digunakan untuk merancang struktur sekunder kompleks target, urutan nukleotida aktual yang akan membentuk struktur yang diinginkan harus dirancang. Desain asam nukleat adalah proses menetapkan urutan basa asam nukleat tertentu untuk setiap untai penyusun struktur agar mereka berasosiasi menjadi konformasi yang diinginkan. Sebagian besar metode bertujuan merancang urutan sedemikian rupa sehingga struktur target memiliki energi terendah, dan dengan demikian paling menguntungkan secara termodinamika, sementara struktur yang terakit secara tidak benar memiliki energi yang lebih tinggi dan karenanya tidak disukai. Hal ini dilakukan baik melalui metode heuristik yang sederhana dan lebih cepat seperti minimalisasi simetri urutan, atau dengan menggunakan model termodinamika tetangga terdekat lengkap, yang lebih akurat namun lebih lambat dan lebih intensif secara komputasi. Model geometris digunakan untuk memeriksa struktur tersier dari nanostruktur tersebut dan untuk memastikan bahwa kompleks tersebut tidak terlalu tegang.[91][93]
Desain asam nukleat memiliki tujuan yang mirip dengan desain protein. Pada keduanya, urutan monomer dirancang untuk mendukung struktur target yang diinginkan dan menghambat pembentukan struktur lain. Desain asam nukleat memiliki keuntungan jauh lebih mudah secara komputasi dibandingkan desain protein, karena aturan pasangan basa yang sederhana sudah cukup untuk memprediksi keuntungan energi suatu struktur, dan informasi rinci tentang pelipatan tiga dimensi keseluruhan dari struktur tersebut tidak diperlukan. Hal ini memungkinkan penggunaan metode heuristik sederhana yang menghasilkan desain yang kuat secara eksperimental. Struktur asam nukleat kurang serbaguna dibandingkan protein dalam fungsinya karena kemampuan protein yang lebih tinggi untuk melipat menjadi struktur yang kompleks, serta terbatasnya keragaman kimia dari empat nukleotida dibandingkan dengan dua puluh asam amino proteinogenik.[93]

Urutan untai DNA yang menyusun struktur target dirancang secara komputasional, menggunakan perangkat lunak pemodelan molekuler dan pemodelan termodinamika.[91][93] Asam nukleat itu sendiri kemudian disintesis menggunakan metode sintesis oligonukleotida standar, yang biasanya diotomatisasi dalam penyintesis oligonukleotida, dan untai dengan urutan kustom tersedia secara komersial.[94] Untai dapat dimurnikan dengan elektroforesis gel denaturasi jika diperlukan,[95] dan konsentrasi yang tepat ditentukan melalui salah satu dari beberapa metode kuantitasi asam nukleat menggunakan spektroskopi serapan ultraviolet.[96]
Struktur target yang terbentuk sepenuhnya dapat diverifikasi menggunakan elektroforesis gel nativ, yang memberikan informasi ukuran dan bentuk untuk kompleks asam nukleat tersebut. Sebuah uji pergeseran mobilitas elektroforesis dapat menilai apakah suatu struktur menggabungkan semua untai yang diinginkan.[97] Pelabelan fluoresen dan transfer energi resonansi Förster (FRET) terkadang digunakan untuk mengarakterisasi struktur kompleks tersebut.[98]
Struktur asam nukleat dapat dicitrakan secara langsung dengan mikroskopi gaya atom, yang sangat cocok untuk struktur dua dimensi yang terentang, namun kurang berguna untuk struktur tiga dimensi diskret karena interaksi ujung mikroskop dengan struktur asam nukleat yang rapuh; mikroskopi elektron transmisi dan mikroskopi krio-elektron sering digunakan dalam kasus ini. Kisi tiga dimensi yang terentang dianalisis dengan kristalografi sinar-X.[99][100]
Umum:
Bidang spesifik: