Fibrodysplasia ossificans progressiva, yang juga dikenal sebagai penyakit Münchmeyer atau sebelumnya disebut myositis ossificans progressiva, merupakan kelainan jaringan ikat yang sangat langka. Kelainan ini dicirikan oleh proses di mana jaringan jaringan ikat fibrosa seperti otot, tendon, dan ligamen mengalami osifikasi bertransmisi menjadi jaringan tulang. Karena pembentukan tulang baru ini menggantikan jaringan otot dan menyatu dengan kerangka tubuh, FOP secara progresif membatasi gerakan pasien hingga menyebabkan imobilitas total. Karena dampaknya yang melumpuhkan, FOP kerap dijuluki sebagai "penyakit manusia batu".
Sumber: Lihat artikel asli di Wikipedia
Artikel ini memiliki beberapa masalah. Tolong bantu memperbaikinya atau diskusikan masalah-masalah ini di halaman pembicaraannya. (Pelajari bagaimana dan kapan saat yang tepat untuk menghapus templat pesan ini)
|
| Fibrodysplasia ossificans progressiva | |
|---|---|
| Nama lain | Penyakit manusia batu (Stone man disease), penyakit Münchmeyer |
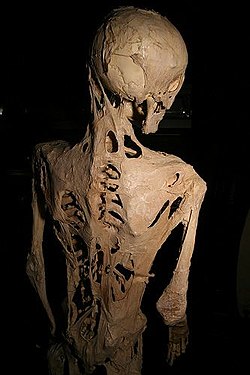 | |
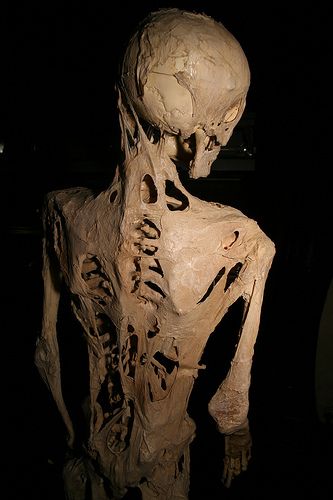
| Kerangka Harry Raymond Eastlack, seorang pasien fibrodysplasia ossificans progressiva, memperlihatkan pertumbuhan tulang abnormal yang khas. | |
| Spesialisasi | Medical genetics, rheumatology |
| Gejala | Pertumbuhan tulang berkelanjutan |
| Awitan umum | Sebelum usia 10 tahun |
| Durasi | Seumur hidup |
| Penyebab | Mutasi pengaktif heterozigot pada gen ACVR1 |
| Metode diagnostik | Osifikasi heterotopik, pengurutan genetik ACVR1 |
| Diagnosis banding | Displasia fibrosa, heteroplasia osseous progresif, |
| Pengobatan | Terapi target dan perawatan suportif |
| Obat | Palovarotene, nama dagang Sohonos |
| Prognosis | Harapan hidup rata-rata sekitar 40 tahun (jika ditangani dengan tepat) |
| Frekuensi | 801 kasus terkonfirmasi di seluruh dunia (2017); tingkat kejadian diperkirakan 0.5 kasus per satu juta orang (1 dari 2 juta) |
| Kematian | 60 |
Fibrodysplasia ossificans progressiva ( /ˌfaɪbroʊdɪˈspleɪʒ(i)ə ɒˈsɪfɪkænz prəˈɡrɛsɪvə/; disingkat FOP), yang juga dikenal sebagai penyakit Münchmeyer atau sebelumnya disebut myositis ossificans progressiva, merupakan kelainan jaringan ikat yang sangat langka. Kelainan ini dicirikan oleh proses di mana jaringan jaringan ikat fibrosa seperti otot, tendon, dan ligamen mengalami osifikasi bertransmisi menjadi jaringan tulang. Karena pembentukan tulang baru ini menggantikan jaringan otot dan menyatu dengan kerangka tubuh, FOP secara progresif membatasi gerakan pasien hingga menyebabkan imobilitas total. Karena dampaknya yang melumpuhkan, FOP kerap dijuluki sebagai "penyakit manusia batu".
Mutasi pada gen ACVR1 adalah penyebab FOP, yang secara langsung mengganggu mekanisme perbaikan alami tubuh. Jaringan fibrosa, mecakup ligamen, tendon, dan otot, dapat mengalami osifikasi (pembentukan tulang), baik secara spontan maupun ketika rusak akibat trauma. Pembentukan tulang baru ini (dikenal sebagai "osifikasi heterotopik") menggantikan jaringan otot yang rusak, dan dalam banyak kasus, cedera yang relatif ringan dapat menyebabkan sendi menyatu secara permanen. Osifikasi heterotopik ini secara bertahap menciptakan kerangka sekunder, yang pada akhirnya membatasi kemampuan gerak pasien. Di samping pertumbuhan tulang yang menjadi ciri khasnya, bukti tidak langsung menunjukkan bahwa kelainan parah dan melumpuhkan ini juga dapat memicu degradasi sendi.
Meskipun terbentuk di lokasi yang tidak seharusnya, tulang yang dihasilkan dari proses osifikasi ini sebenarnya identik dengan tulang "normal". Tingkat pertumbuhan tulang yang mengalami osifikasi bervariasi antara satu pasien dengan pasien lainnya. FOP merupakan satu-satunya kondisi medis yang diketahui di mana jaringan dari satu sistem organ dapat berubah menjadi jaringan dari sistem organ lain.
Saat ini, belum ada obat yang diketahui untuk FOP. Risiko bedah harus diperhatikan; area yang mengalami osifikasi justru diperbaiki oleh tubuh dengan menghasilkan tulang tambahan jika tulang tersebut diangkat. Meskipun demikian, pengobatan intermiten seperti obat anti-inflamasi tersedia. Di antara terobosan menjanjikan, terdapat pengobatan yang telah disetujui, Sohonos (palovarotene), serta terapi dimediasi Antisense dengan LNA gapmers yang selektif alel.
Pada tahun 1692, laporan medis yang menjelaskan individu penderita FOP berasal dari Dr. Guy Patin. [1] FOP awalnya disebut myositis ossificans progressiva dan dianggap disebabkan oleh peradangan otot (myositis) yang menyebabkan pembentukan tulang. [1] Seorang ahli bedah London, John Freke, pada tahun 1736, menulis laporan kasus FOP yang pertama, menggambarkan seorang anak laki-laki berusia 14 tahun yang menunjukkan 'banyak pembengkakan besar di punggungnya, yang muncul dari semua tulang belakang leher dan mencapai os sacrum. Pembengkakan tersebut juga muncul dari setiap tulang rusuk tubuhnya, dan menyatuh di seluruh bagian punggungnya, seperti percabangan koral, membentuk, seolah-olah, sepasang korset tulang yang kaku." Penyakit ini dinamai ulang oleh Victor A. McKusick pada tahun 1970 setelah ditemukannya bahwa jaringan lunak selain otot (misalnya, ligamen) juga dipengaruhi oleh proses penyakit tersebut. [1]
Kasus yang melibatkan Harry Eastlack (1933–1973) adalah kasus FOP yang paling terkenal. Kondisinya mulai memburuk saat ia berusia sepuluh tahun. Menjelang kematiannya akibat pneumonia pada November 1973, enam hari sebelum ulang tahunnya yang ke-40, tubuhnya telah mengalami osifikasi total, membuatnya hanya mampu menggerakkan bibirnya. Selama hidupnya, Eastlack tidak pernah bertemu dengan sesama penderita FOP.
Kerangka Harry Eastlack kini berfungsi sebagai sumber informasi yang sangat berharga dalam studi FOP; kerangka tersebut berada di Museum Mütter di Philadelphia, setelah ia mendonasikan tubuhnya untuk kepentingan ilmu pengetahuan. Penderita FOP lainnya, Carol Orzel (lahir 20 April 1959, meninggal Februari 2018), juga mewariskan tubuhnya kepada museum yang sama. Sejak Februari 2019, kerangka Carol Orzel dapat dilihat dalam pameran di sana, diposisikan berdekatan dengan kerangka Eastlack [2]
Tercatat hingga tahun 2017, terdapat sekitar 800 kasus FOP yang telah dikonfirmasi di seluruh dunia, menjadikannya salah satu penyakit terlangka yang ada. Kelainan ini memengaruhi semua etnis, dengan estimasi insiden sebesar 0,5 kasus untuk setiap juta populasi.[3]
FOP disebabkan oleh alel dominan autosomal pada kromosom 2q23-24.[4] Alel ini memiliki ekspresivitas bervariasi, tetapi penetrasinya lengkap. Sebagian besar kasus disebabkan oleh mutasi spontan pada gamet ; kebanyakan orang dengan FOP tidak dapat atau memilih untuk tidak memiliki anak. Adapun penyakit serupa tetapi tidak terlalu fatal adalah displasia fibrosa, yang disebabkan oleh mutasi pasca-zigotik .
Mutasi pada gen ACVR1 (juga dikenal sebagai activin-like kinase 2 (ALK2)) bertanggung jawab atas penyakit ini. [4] ACVR1 mengkodekan reseptor aktivin tipe-1, reseptor BMP tipe-1. Mutasi tersebut menyebabkan substitusi kodon 206 dari arginin menjadi histidin dalam protein ACVR1. [5] Substitusi ini menyebabkan aktivasi abnormal ACVR1, yang mengarah pada transformasi jaringan ikat dan jaringan otot menjadi kerangka sekunder. Hal ini menyebabkan sel endotel bertransformasi menjadi sel punca mesenkimal (mesenchymal stem cells) dan kemudian menjadi tulang. [6] Normalnya, gen ACVR1 mengkodekan reseptor aktivin tipe-1 transmembran kinase yang mengikat reseptor BMP (BMPR Tipe I dan BMPR Tipe II) untuk pensinyalan kondrogenesis . BMP termasuk dalam superfamili protein yang dikenal sebagai protein Faktor pertumbuhan transformasi beta (TGF- <b id="mwnw">β</b>). Pengikatan protein ACVR1 ke reseptor BMP memulai kaskade sinyal yang sangat penting untuk menginduksi pembentukan tulang endokondral selama perkembangan, serta homeostasis kerangka dan jaringan. [7]

Kelainan ini diwariskan secara autosomal dominan. Dengan demikian, seorang anak memiliki probabilitas 50% untuk mewarisi FOP jika salah satu orang tua adalah heterozigot yang terdampak. Meskipun dua individu yang menderita FOP dapat menghasilkan anak yang sehat, mutasi gen baru memungkinkan dua individu yang tidak terdampak memiliki keturunan yang menderita FOP. Perlu dicatat bahwa bentuk homozigot dominan menunjukkan tingkat keparahan yang lebih tinggi dibandingkan dengan bentuk heterozigot.
Protein yang menyebabkan osifikasi normalnya dinonaktifkan oleh protein penghambat setelah tulang janin terbentuk di dalam rahim, tetapi pada pasien FOP, protein tersebut terus bekerja. Pembentukan tulang menyimpang (aberrant) pada pasien FOP terjadi ketika jaringan ikat atau sel otot yang terluka di lokasi cedera atau pertumbuhan secara keliru mengekspresikan enzim untuk perbaikan tulang selama apoptosis (kematian sel yang diatur sendiri). Hal ini menghasilkan limfosit yang mengandung kelebihan protein morfogenetik tulang 4 (BMP4) yang disediakan selama respons sistem imun. Tulang yang dihasilkan terjadi secara independen dari kerangka normal, membentuk elemen kerangkanya sendiri yang terpisah. Namun, elemen-elemen ini dapat menyatu dengan tulang kerangka normal[8]. Diafragma, lidah, dan otot ekstra-okular terselamatkan dalam proses ini, begitu pula otot jantung dan otot polos.[9]. Karena enzim yang keliru tetap tidak terselesaikan dalam respons imun, tubuh terus menyediakan limfosit yang mengandung BMP4 yang salah. BMP4 adalah produk yang berkontribusi pada perkembangan kerangka pada embrio normal.[10]
Kelainan FOP terjadi ketika gen ACVR1 bermutasi. Gen yang mengodekan reseptor protein morfogenetik tulang (BMP) ini berfungsi mengatur pertumbuhan dan perkembangan otot dan tulang. Mutasi khas R202H mengurangi efisiensi penghambatan, sebab molekul FKBP1A mengikat GS-loop aktivasi dengan lemah.[11] Karena ACVR1 gagal dimatikan secara efektif, pasien mengalami pertumbuhan tulang rawan dan tulang yang berlebihan, serta penyatuan sendi.[12] Mutasi yang melibatkan residu lain bekerja dengan cara yang mirip. Dalam beberapa kasus, reseptor bahkan dapat memberi sinyal bahwa ia aktif meskipun ligan aktivasinya tidak terikat.[13]
Sebagian besar kasus FOP merupakan hasil dari mutasi gen baru; artinya, individu yang terkena tidak memiliki riwayat kelainan spesifik ini dalam garis keturunan keluarga mereka. Walaupun demikian, terdapat sejumlah kecil kasus di mana mutasi tersebut diwarisi dari salah satu orang tua yang menderita FOP
Untuk alasan yang tidak diketahui, anak-anak yang lahir dengan FOP seringkali menunjukkan malformasi pada jempol kaki, Hal ini kadang ditandai dengan hilangnya sendi atau, dalam kasus lain, hanya berupa benjolan yang terlihat jelas pada sendi minor.[19] "Kekambuhan" pertama yang mengarah pada pembentukan tulang FOP biasanya terjadi sebelum usia 10 tahun.[19] Pertumbuhan tulang ini umumnya berkembang dari atas tubuh ke bawah, sama seperti pertumbuhan tulang pada janin. Anak dengan FOP biasanya akan mulai mengembangkan tulang tambahan mulai dari leher, kemudian berlanjut di bahu, lengan, area dada, dan terakhir pada kaki.
Osifikasi pada umumnya mulai terjadi di bagian dorsal, aksial, kranial, dan proksimal tubuh. Kemudian, penyakit ini bergerak maju, melibatkan daerah ventral, apendikular, kaudal, dan distal.[20] Pola perkembangan ini bisa terganggu karena seringnya terjadi kekambuhan yang diakibatkan cedera. Kekambuhan ini ditandai oleh kemunculan benjolan menyerupai tumor secara mendadak.
Pertumbuhan tulang yang terjadi selama kekambuhan dapat menyebabkan hilangnya mobilitas sendi yang terdampak. Jika rahang/mandibula terlibat, pasien akan mengalami ketidakmampuan untuk membuka mulut sepenuhnya, yang membatasi kemampuan berbicara dan makan. Selain itu, pertumbuhan tulang di sekitar pinggul atau lutut dapat menyebabkan imobilisasi total, memengaruhi kemampuan berjalan. Yang lebih serius, pembentukan tulang ekstra di sekitar tulang rusuk membatasi pengembangan paru-paru dan diafragma, sehingga menimbulkan komplikasi pernapasan.[19]
Dengan tingkat kejadian hanya 1 dari 2 juta orang, FOP termasuk kelainan yang sangat jarang ditemukan. Karena kelangkaannya, FOP seringkali salah didiagnosis sebagai kanker atau fibrosis. Dokter perlu menghindari biopsi, sebab prosedur tersebut berisiko memicu pertumbuhan tulang FOP yang lebih parah. Untungnya, keberadaan jari kaki atau ibu jari yang cacat sejak lahir pada penderita FOP membantu membedakan kondisi ini dari masalah kerangka yang lain[21]
Dengan penanganan medis yang tepat, usia rata-rata kelangsungan hidup adalah 40 tahun. Namun, diagnosis yang terlambat, trauma, dan infeksi dapat menurunkan harapan hidup.
FOP didiagnosis berdasarkan kombinasi fitur klinis, studi pencitraan, dan pengujian genetik. Ciri klinis utama FOP meliputi malformasi kongenital (congenital malformations) pada ibu jari kaki besar (hallux valgus) dan episode pembengkakan jaringan lunak yang menyakitkan. Ciri-ciri khas FOP pada radiograf dan pemindaian CT mencakup pembentukan tulang ekstraosseous dalam jaringan lunak, membentuk tulang berkorteks dalam pita, lembaran, atau jembatan melintasi sendi. Selama kekambuhan, MRI dan USG sensitif untuk lesi pra-osseous, termasuk edema jaringan lunak dan penyengatan (enhancement) sebelum terjadi osifikasi. Pemindaian PET dapat mengidentifikasi lesi awal yang aktif secara metabolik, dan dapat memprediksi lokasi osifikasi di masa depan. Pengujian genetik molekuler untuk FOP mencakup analisis urutan gen .
Diagnosis dini kelainan ini melalui radiologi sangat penting untuk menghindari pemeriksaan invasif yang tidak perlu seperti biopsi . Trauma kecil atau sepele atau suntikan intramuskular dapat memperparah progresi penyakit melalui peradangan, sehingga radiologi lebih disukai. Dokter harus mewaspadai entitas langka ini, karena sering salah didiagnosis sebagai kanker atau entitas jinak lainnya seperti infeksi, sehingga biopsi seringkali dapat mempercepat progresi penyakit.
Secara khusus, upaya pengangkatan tulang secara bedah pada pasien FOP dapat memicu pertumbuhan tulang baru yang eksplosif. Saat menjalani anestesi, penderita FOP mungkin mengalami kesulitan dengan intubasi, penyakit paru restriktif, dan perubahan pada sistem konduksi listrik jantung. Kegiatan yang meningkatkan risiko jatuh atau cedera jaringan lunak harus dihindari, karena trauma ringan sekalipun, termasuk suntikan intramuskular (misalnya, imunisasi), harus dihindari karena dapat memicu osifikasi heterotopik.
Saat ini, operasi biasanya tidak direkomendasikan bagi penderita FOP karena dapat memicu pembentukan tulang yang cepat di lokasi sayatan atau di lokasi jahitan yang diterapkan pada otot atau jaringan ikat. Operasi penyelamatan jiwa dapat dipertimbangkan, namun menyusun rencana bedah dengan masukan dari spesialis FOP dapat dianggap sebagai praktik terbaik. Pelepasan kontraktur sendi secara bedah umumnya tidak berhasil dan berisiko memicu osifikasi heterotopik baru akibat trauma.
Saat ini, belum ditemukan obat untuk FOP dan belum ada pengobatan definitif yang terbukti efektif. Meskipun demikian, pasien dapat menjalani terapi intermiten. Terapi ini melibatkan pemberian obat anti-inflamasi untuk menekan respons peradangan akibat kekambuhan atau peradangan yang timbul dari kerusakan otot.
Terobosan yang menjanjikan terletak pada Sohonos (palovarotene), terapi pertama yang disetujui FDA untuk FOP. Sohonos adalah agonis reseptor asam retinoat gamma (RARγ) yang sangat selektif dan telah terbukti mengurangi volume osifikasi heterotopik baru pada pasien (laki-laki >10 tahun, perempuan >8 tahun). Data keamanan obat jangka panjang telah menunjukkan bahwa efek samping terkait retinoid umum terjadi pada terapi Sohonos. Efek samping ini mencakup penutupan fisis prematur pada pasien yang kerangkanya belum matang, penurunan kepadatan tulang vertebra, dan peningkatan risiko patah tulang.
Uji klinis yang melibatkan isotretinoin, etidronate dengan kortikosteroid oral, dan perhexiline maleate belum berhasil menunjukkan efektivitas. Walaupun demikian, hasil ini tetap menyisakan ketidakpastian, terutama karena perjalanan penyakit FOP yang bervariasi dan prevalensinya yang rendah [6]
Kini, sejumlah farmasi yang berkonsentrasi pada penemuan obat untuk kelainan genetik yang jarang sedang menjalani tingkat penelitian yang berbeda-beda dalam upaya mencari solusi pengobatan yang beragam bagi FOP.
Status obat orphan untuk dua senyawa baru bagi FOP diberikan oleh Kantor Pengembangan Produk Orphan (Orphan Products Development) Badan Pengawas Obat dan Makanan AS (FDA) kepada La Jolla Pharmaceuticals pada Agustus 2015. Senyawa-senyawa tersebut merupakan inhibitor protein kinase molekul kecil yang dirancang untuk memblokir ACVR1 (ALK2) secara selektif. [7]
Palovarotene, yang merupakan agonis reseptor asam retinoat gamma, telah menunjukkan potensi besar dalam studi praklinis. Dalam model hewan, obat ini terbukti memblokir pembentukan tulang abnormal dengan cara menghambat sistem secondary messenger dalam jalur BMP.[8] Pada Agustus 2015, Clementia Pharmaceuticals, yang melisensikan palovarotene dari Roche Pharmaceuticals, mulai mendaftarkan anak-anak (usia 6 tahun ke atas) untuk uji klinis Fase II dalam pengobatan FOP.[9] Palovarotene telah dievaluasi oleh Roche pada lebih dari 800 individu (termasuk sukarelawan sehat dan pasien PPOK) sebelum dilisensikan. Karena potensinya, obat ini mendapat Fast Track designation dari FDA, dan penetapan obat orphan dari FDA dan European Medicines Agency (EMA).[10] Dalam uji coba penting Fase 3 MOVE yang dipublikasikan tahun 2023, Sohonos (nama dagang palovarotene) terbukti mengurangi osifikasi heterotopik baru sebesar 54–60%.[11]
Aktivasi reseptor ACVR1 oleh aktivin A terungkap sebagai mekanisme penting dalam penyakit ini, sesuai dengan wawasan baru yang diumumkan oleh Regeneron pada September 2015. Selanjutnya, studi fase 1 dari antibodi aktivin perusahaan, REGN 2477, dimulai pada tahun 2016 pada sukarelawan sehat; diikuti oleh uji coba fase 2 yang dilakukan pada pasien FOP di tahun 2017.
Pengobatan menjanjikan lainnya adalah terapi yang dimediasi Antisense, khususnya menggunakan LNA gapmers yang selektif alel. [12] Interferensi RNA yang spesifik alel menargetkan mRNA yang bermutasi untuk didegradasi sambil mempertahankan ekspresi gen ACVR1 normal. [13] Pendekatan ini menargetkan gen ACVR1 yang bermutasi, yang menyebabkan osifikasi heterotopik dengan merespons terhadap aktivin A secara abnormal. Dalam studi terbaru, LNA gapmers secara efektif mengurangi ekspresi transkrip ACVR1R206H patogenik sambil menyelamatkan gen ACVR1 tipe liar, sehingga secara selektif menekan diferensiasi osteogenik yang terkait dengan FOP. Pendekatan antisense baru ini menawarkan potensi untuk aplikasi terapeutik pada FOP, yang mewakili terobosan dalam pengobatan genetik yang ditargetkan untuk gangguan ini dan berpotensi kelainan autosomal dominan lainnya.
Mekanisme pembentukan tulang heterotopik pada FOP perlu diselidiki lebih lanjut karena hasil investigasi tersebut berpotensi membantu pengembangan terapi bagi gangguan lain yang melibatkan pembentukan tulang di luar kerangka normal.
Sel Fibro/adipogenic progenitors (FAPs) dispekulasikan sebagai jenis sel yang bertanggung jawab atas pembentukan tulang ektopik (ekstra-kerangka) yang diaktifkan oleh aktivin A. Fenomena ini teramati pada otot dan tendon tikus yang memiliki mutasi ACVR1(R206H), mutasi penyebab FOP.[14]
Ipsen mengeluarkan penangguhan klinis sebagian (partial clinical hold) pada Desember 2019. Keputusan ini hanya berlaku untuk pasien di bawah usia 14 tahun, menyusul adanya laporan mengenai fusi dini pada lempeng pertumbuhan.
Hingga pembaruan data tahun 2021, saracatinib, sebuah kandidat terapi yang potensial, telah memasuki uji klinis fase III. Obat ini dikembangkan sebagai penghambat osifikasi heterotopik yang kuat pada tikus wild-type dan tikus mutan ACVR1.