Besi (II) sulfida adalah senyawa kimia dengan rumus FeS. Dalam praktik, besi sulfida sering kali bersifat non-stoikiometrik.
Sumber: Lihat artikel asli di Wikipedia

 | |
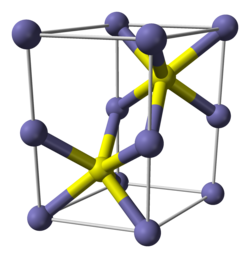 | |
| Penanda | |
|---|---|
Model 3D (JSmol) |
|
| ChemSpider |
|
| Nomor EC | |
PubChem CID |
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA) |
|
| |
| |
| Sifat | |
| FeS | |
| Massa molar | 87.910 g/mol |
| Densitas | 4.84 g/cm3 |
| Titik lebur | 1194 °C |
| Kelarutan | bereaksi dalam asam |
| Bahaya | |
| Bahaya utama | bisa jadi piroforik |
| Senyawa terkait | |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Besi (II) sulfida adalah senyawa kimia dengan rumus FeS. Dalam praktik, besi sulfida sering kali bersifat non-stoikiometrik.
Besi sulfida ada dalam beberapa bentuk yang berbeda:
Besi sulfida bereaksi dengan asam hidroklorik dan menghasilkan hidrogen sulfida yang sangat beracun
FeS dapat diperoleh dengan memanaskan besi dan sulfur:
Belle Lowe (1937), "The formation of ferrous sulfide in cooked eggs", Experimental cookery from the chemical and physical standpoint, John Wiley & Sons