Oksidase xantina adalah bentuk oksidoreduktase xantina, sejenis enzim yang menghasilkan spesies oksigen reaktif. Enzim-enzim ini mengkatalisis oksidasi hipoksantina menjadi xantina dan selanjutnya dapat mengkatalisis oksidase xantina menjadi asam urat. Enzim-enzim ini memainkan peran penting dalam katabolisme purin pada manusia dan beberapa hewan.
Sumber: Lihat artikel asli di Wikipedia
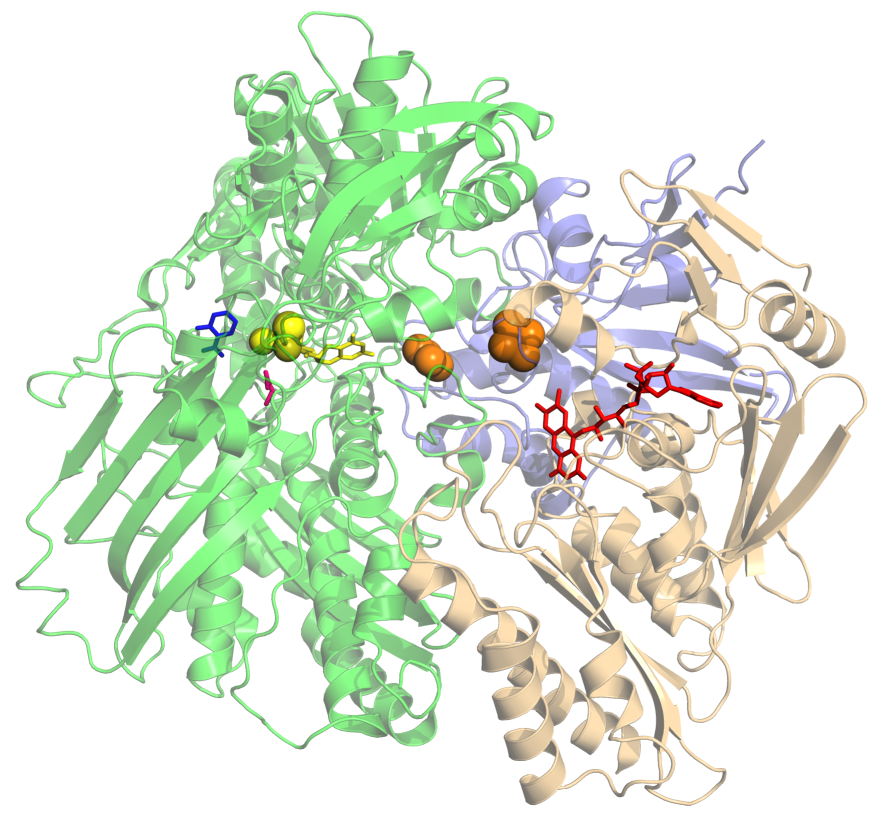
| Oksidase/dehidrogenase xantina | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Pengidentifikasi | |||||||||
| Nomor EC | 1.17.3.2 | ||||||||
| Nomor CAS | 9002-17-9 | ||||||||
| Basis data | |||||||||
| IntEnz | tinjauan IntEnz | ||||||||
| BRENDA | entri BRENDA | ||||||||
| ExPASy | tinjauan NiceZyme | ||||||||
| KEGG | entri KEGG | ||||||||
| MetaCyc | jalur metabolik | ||||||||
| PRIAM | profil | ||||||||
| Struktur PDB | RCSB PDB PDBe PDBsum | ||||||||
| Ontologi Gen | AmiGO / EGO | ||||||||
| |||||||||
| Oksidase/dehidrogenase xantina | |||||||
|---|---|---|---|---|---|---|---|
| Pengidentifikasi | |||||||
| Simbol | XDH | ||||||
| Gen NCBI | 7498 | ||||||
| HGNC | 12805 | ||||||
| OMIM | 607633 | ||||||
| PDB | 1FIQ | ||||||
| RefSeq | NM_000379 | ||||||
| UniProt | P47989 | ||||||
| Data lain | |||||||
| Nomor EC | 1.17.3.2 | ||||||
| Lokus | Chr. 2 p23.1 | ||||||
| |||||||
Oksidase xantina (Bahasa Inggris: Xanthine oxidase, disingkat XO atau XAO) adalah bentuk oksidoreduktase xantina, sejenis enzim yang menghasilkan spesies oksigen reaktif.[2] Enzim-enzim ini mengkatalisis oksidasi hipoksantina menjadi xantina dan selanjutnya dapat mengkatalisis oksidase xantina menjadi asam urat. Enzim-enzim ini memainkan peran penting dalam katabolisme purin pada manusia dan beberapa hewan.[3]
Oksidase xantina didefinisikan sebagai aktivitas enzim (EC 1.17.3.2).[4] Protein yang sama, yang pada manusia memiliki simbol gen XDH yang disetujui HGNC, juga dapat memiliki aktivitas dehidrogenase xantina (EC 1.17.1.4).[5] Sebagian besar protein di hati ada dalam bentuk dengan aktivitas dehidrogenase xantina, tetapi dapat diubah menjadi oksidase xantina melalui oksidasi sulfhidril reversibel atau melalui modifikasi proteolitik ireversibel.[6][7]
Reaksi kimia berikut dikatalisis oleh oksidase xantina:
Karena XO adalah enzim penghasil superoksida, dengan spesifisitas umum yang rendah,[9] enzim ini dapat dikombinasikan dengan senyawa dan enzim lain dan menghasilkan oksidan reaktif, serta mengoksidasi substrat lain.
Oksidase xantina bovinae (dari susu) awalnya dianggap memiliki situs pengikatan untuk mereduksi sitokrom c, tetapi telah ditemukan bahwa mekanisme untuk mereduksi protein ini adalah melalui produk sampingan anion superoksida XO, dengan penghambatan kompetitif oleh anhidrase karbonat.[10]
Reaksi lain yang dikatalisis oleh oksidase xantina adalah dekomposisi S-nitrosotiol (RSNO), suatu golongan spesies nitrogen reaktif, menjadi nitrogen monoksida (NO), yang bereaksi dengan anion superoksida membentuk peroksinitrit dalam kondisi aerobik.[11]
XO juga ditemukan menghasilkan anion radikal karbonat oksidan satu elektron yang kuat dari oksidasi dengan asetaldehida dengan adanya katalase dan bikarbonat. Diduga bahwa radikal karbonat tersebut kemungkinan besar diproduksi di salah satu pusat redoks enzim dengan zat antara peroksimonokarbonat.[9]
Berikut adalah diagram yang menyoroti jalur-jalur yang dikatalisis oleh oksidase xantina.

Diduga bahwa oksidoreduktase xantina, bersama dengan enzim lain, berperan dalam konversi nitrat menjadi nitrit dalam jaringan manusia dan mamalia.[12]
Situs aktif XO terdiri dari unit molibdopterin dengan atom molibdenum juga dikoordinasikan oleh oksigen terminal (oxo), atom belerang dan hidroksida terminal. Dalam reaksi dengan xantina untuk membentuk asam urat, gugus S=MoVIO-H terionisasi dan MoVI-O− yang dihasilkan menyerang karbon bersamaan dengan transfer H− ke Mo=S. Pusat HS-MoIV-O-C yang dihasilkan kemudian mengalami oksidasi 2e dengan hidrolisis gugus MoVI-O-C, menghasilkan kembali S=MoVI-OH, bersama dengan xantina.[3]
Oksidase xantina adalah enzim penghasil superoksida yang ditemukan secara normal dalam serum darah dan paru-paru, dan aktivitasnya meningkat selama infeksi virus influenza A.[13]
Selama kerusakan hati yang parah, oksidase xantina dilepaskan ke dalam darah, sehingga pemeriksaan darah untuk XO merupakan cara untuk menentukan apakah telah terjadi kerusakan hati.[14]
Karena oksidase xantina merupakan lintasan metabolisme untuk pembentukan asam urat, penghambat oksidase xantina alopurinol, digunakan dalam pengobatan encok. Karena oksidase xantina terlibat dalam metabolisme 6-merkaptopurin, kehati-hatian harus dilakukan sebelum memberikan alopurinol dan 6-merkaptopurin, atau bakal obatnya yakni azatioprin, secara bersamaan.
Xantinuria adalah kelainan genetik langka di mana kekurangan oksidase xantina menyebabkan konsentrasi xantina yang tinggi dalam darah dan dapat menyebabkan masalah kesehatan seperti gagal ginjal. Tidak ada pengobatan khusus, orang yang terkena disarankan oleh dokter untuk menghindari makanan tinggi purin dan untuk menjaga asupan cairan yang tinggi. Xantinuria tipe I telah ditelusuri langsung ke mutasi gen XDH yang memediasi aktivitas oksidase xantina. Xantinuria tipe II dapat terjadi akibat kegagalan mekanisme yang memasukkan belerang ke dalam situs aktif oksidase xantina dan oksidase aldehida, enzim terkait dengan beberapa aktivitas yang tumpang tindih (seperti konversi alopurinol menjadi oksipurinol).[15]
Penghambatan oksidase xantina telah diusulkan sebagai mekanisme untuk meningkatkan kesehatan kardiovaskular.[16] Sebuah studi menemukan bahwa pasien dengan penyakit paru obstruktif kronik (PPOK) mengalami penurunan stres oksidatif, termasuk oksidasi glutation dan peroksidasi lipid, ketika oksidase xantina dihambat menggunakan alopurinol.[17] Stres oksidatif dapat disebabkan oleh radikal bebas hidroksil dan hidrogen peroksida, yang keduanya merupakan produk sampingan dari aktivitas XO.[18]
Peningkatan konsentrasi asam urat serum telah diteliti sebagai indikator faktor kesehatan kardiovaskular, dan telah digunakan untuk memprediksi mortalitas, transplantasi jantung, dan lainnya pada pasien.[16] Namun, belum jelas apakah hal ini dapat menjadi hubungan langsung atau tidak langsung antara konsentrasi asam urat serum (dan melalui proksi, aktivitas oksidase xantina) dan kesehatan kardiovaskular.[19] Kondisi pergantian sel yang tinggi dan konsumsi alkohol merupakan beberapa kasus yang paling menonjol dari konsentrasi asam urat serum yang tinggi.[18]
Spesies nitrogen reaktif seperti peroksinitrit yang dapat dibentuk oleh oksidase xantina, telah ditemukan bereaksi dengan DNA, protein, dan sel, menyebabkan kerusakan sel atau bahkan toksisitas. Pensinyalan nitrogen reaktif, yang digabungkan dengan spesies oksigen reaktif, telah ditemukan sebagai bagian penting dari fungsi miokardium dan vaskular, menjelaskan mengapa oksidase xantina sedang diteliti kaitannya dengan kesehatan kardiovaskular.[20]
Baik oksidase xantina maupun xantin oksidoreduktase xantina juga terdapat pada epitel dan endotel kornea dan mungkin terlibat dalam cedera mata oksidatif.[21]
Penghambat oksidase xantina meliputi alopurinol,[22] oksipurinol,[23] dan asam fitat.[24] Senyawa ini juga ditemukan dihambat oleh flavonoid,[25] termasuk flavonoid yang terdapat dalam daun Bougainvillea spectabilis (famili Nyctaginaceae, dengan IC50 sebesar 7,23 μM), yang umumnya digunakan dalam pengobatan tradisional.[26]