Budesonid/formoterol adalah obat kombinasi dosis tetap yang digunakan dalam pengelolaan asma atau penyakit paru obstruktif kronik (PPOK). Obat ini mengandung budesonid dan formoterol. Monografi produk tidak mendukung penggunaannya untuk perburukan mendadak atau pengobatan bronkospasme aktif. Namun, tinjauan literatur tahun 2020 mendukung penggunaan tersebut. Obat ini digunakan dengan cara dihirup.
Sumber: Lihat artikel asli di Wikipedia
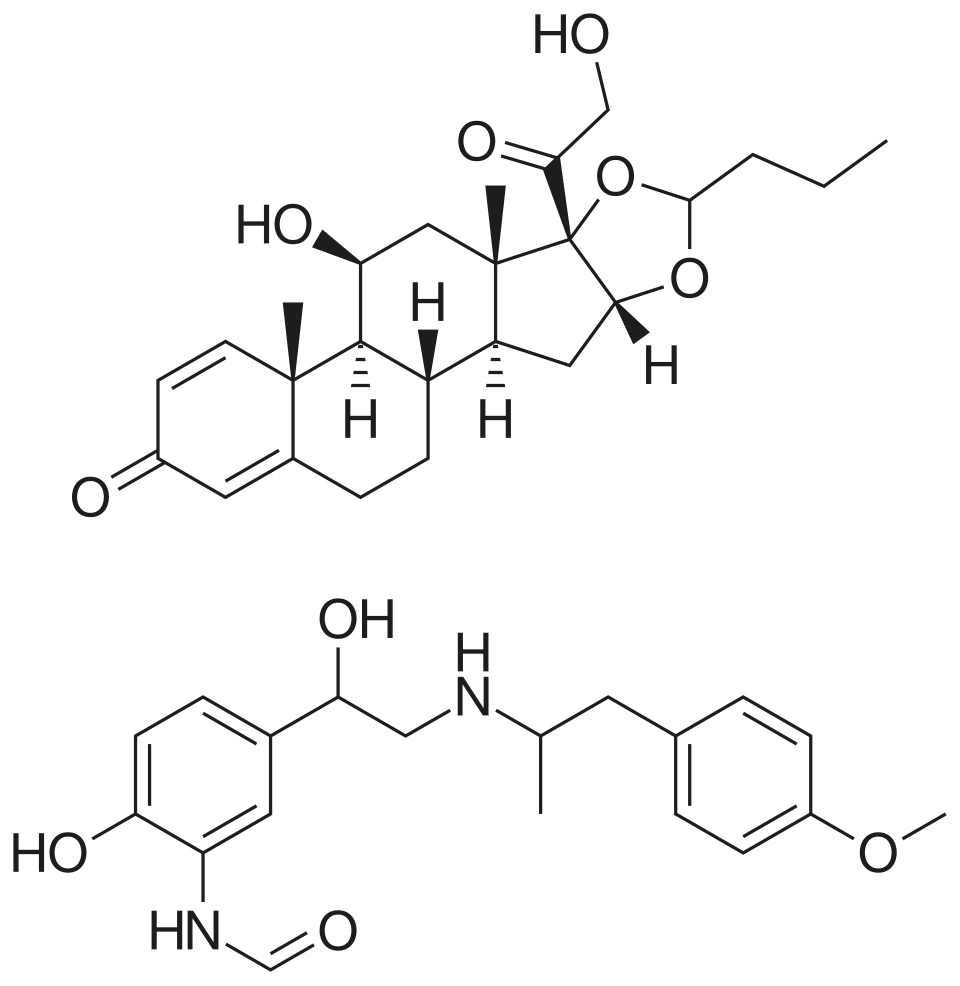
 | |
| Kombinasi dari | |
|---|---|
| Budesonid | Glukokortikoid |
| Formoterol | Agonis beta-adrenoseptor kerja panjang |
| Data klinis | |
| Nama dagang | Symbicort, dll |
| AHFS/Drugs.com | |
| MedlinePlus | a623022 |
| License data | |
| Kategori kehamilan | |
| Rute pemberian | Inhalasi[2] |
| Kode ATC | |
| Status hukum | |
| Status hukum | |
| Pengenal | |
| Nomor CAS | |
| KEGG | |
| CompTox Dashboard (EPA) | |
| (verify) | |
Budesonid/formoterol adalah obat kombinasi dosis tetap yang digunakan dalam pengelolaan asma atau penyakit paru obstruktif kronik (PPOK). Obat ini mengandung budesonid (suatu kortikosteroid) dan formoterol (suatu agonis β2 kerja lama atau LABA). Monografi produk tidak mendukung penggunaannya untuk perburukan mendadak atau pengobatan bronkospasme aktif.[2] Namun, tinjauan literatur tahun 2020 mendukung penggunaan tersebut.[6] Obat ini digunakan dengan cara dihirup.[2]
Efek samping yang umum (≥1/100 hingga <1/10) meliputi kandidiasis, sakit kepala, tremor, palpitasi, iritasi tenggorokan, batuk, dan suara serak.[7] Pneumonia merupakan efek samping yang umum pada orang dengan PPOK, dan efek samping lain yang kurang umum telah didokumentasikan.[2][3] Ada kekhawatiran bahwa komponen LABA meningkatkan risiko kematian pada anak-anak dengan asma, tetapi kekhawatiran ini telah dihilangkan pada tahun 2017.[8] Oleh karena itu, kombinasi ini hanya direkomendasikan pada mereka yang tidak terkontrol dengan steroid inhalasi saja.[2] Ada bukti sementara bahwa dosis umum steroid inhalasi dan LABA aman untuk kehamilan.[9] Formoterol dan budesonid keduanya diekskresikan dalam ASI.[1]
Budesonid/formoterol disetujui untuk penggunaan medis di Amerika Serikat pada tahun 2006.[2][10] Obat ini masuk dalam Daftar Obat Esensial Organisasi Kesehatan Dunia.[11][12] Obat ini tersedia sebagai obat generik.[13]
Budesonid/formoterol diindikasikan untuk pengobatan asma dan untuk pengobatan pemeliharaan obstruksi aliran udara dan mengurangi eksaserbasi pada orang dengan penyakit paru obstruktif kronik.[2][4][5]
Budesonid/formoterol telah menunjukkan efikasi untuk mencegah serangan asma.[6] Tidak jelas apakah efikasi budesonid/formoterol berbeda dari flutikason/salmeterol pada asma kronis.[14]
Kombinasi ini disetujui di Amerika Serikat hanya sebagai pengobatan pemeliharaan pada asma dan penyakit paru obstruktif kronik (PPOK).[2] Namun, tinjauan pustaka tahun 2020 mendukung penggunaan sesuai kebutuhan selama perburukan akut pada mereka dengan penyakit ringan, dan sebagai pemeliharaan diikuti dengan dosis tambahan selama perburukan.[6]
Penggunaan untuk pemeliharaan dan pengobatan sesuai kebutuhan juga dikenal sebagai terapi pemeliharaan dan pereda tunggal (SMART) dan merupakan pengobatan yang sudah mapan. Telah terbukti bahwa, 1) mengurangi eksaserbasi asma yang memerlukan kortikosteroid oral, 2) mengurangi kunjungan ke rumah sakit lebih baik daripada pemeliharaan pada kortikosteroid inhalasi saja pada dosis yang lebih tinggi, atau 3) kortikosteroid inhalasi pada dosis yang sama atau lebih tinggi bersama dengan bronkodilator kerja lama (LABA), dengan bronkodilator kerja pendek (SABA) sebagai pelega.[15][16]
Sering kali ringan, dan biasanya hilang saat obat terus digunakan:
Bronkospasme (pengencangan otot di saluran napas yang menyebabkan mengi segera setelah penggunaan obat, yang mungkin merupakan tanda reaksi alergi dan harus segera ditangani dengan perhatian medis)
Dengan dosis tinggi untuk jangka waktu lama.
Budesonid/formoterol disetujui untuk digunakan di Amerika Serikat pada bulan Juli 2006.[2][10][19]
Budesonid/formoterol disetujui untuk digunakan di Uni Eropa pada bulan April 2014.[4][5]
Ada beberapa paten yang terkait dengan obat ini; beberapa di antaranya telah kedaluwarsa.[20] Obat ini awalnya dipasarkan oleh AstraZeneca.
Obat ini dijual dengan berbagai nama merek termasuk Symbicort,[2] BiResp Spiromax,[4] dan DuoResp Spiromax.[5]
evidence for safety of usual doses of ICS and LABA