Analog keadaan transisi adalah senyawa kimia dengan struktur kimia yang menyerupai keadaan transisi molekul substrat dalam reaksi kimia yang dikatalisis enzim. Enzim berinteraksi dengan substrat melalui regangan atau distorsi, menggerakkan substrat menuju keadaan transisi. Analog keadaan transisi dapat digunakan sebagai penghambat dalam reaksi yang dikatalisis enzim dengan memblokir situs aktif enzim. Teori menunjukkan bahwa penghambat enzim yang menyerupai struktur keadaan transisi akan mengikat enzim lebih kuat daripada substrat sebenarnya. Contoh obat yang merupakan penghambat analog keadaan transisi termasuk obat flu seperti penghambat neuraminidase oseltamivir dan penghambat protease HIV sakuinavir dalam pengobatan AIDS.
Sumber: Lihat artikel asli di Wikipedia
Analog keadaan transisi adalah senyawa kimia dengan struktur kimia yang menyerupai keadaan transisi molekul substrat dalam reaksi kimia yang dikatalisis enzim. Enzim berinteraksi dengan substrat melalui regangan atau distorsi, menggerakkan substrat menuju keadaan transisi.[1] Analog keadaan transisi dapat digunakan sebagai penghambat dalam reaksi yang dikatalisis enzim dengan memblokir situs aktif enzim. Teori menunjukkan bahwa penghambat enzim yang menyerupai struktur keadaan transisi akan mengikat enzim lebih kuat daripada substrat sebenarnya.[2] Contoh obat yang merupakan penghambat analog keadaan transisi termasuk obat flu seperti penghambat neuraminidase oseltamivir dan penghambat protease HIV sakuinavir dalam pengobatan AIDS.

Keadaan transisi suatu struktur paling baik dijelaskan dalam kaitannya dengan mekanika statistika di mana energi ikatan yang putus dan terbentuk memiliki probabilitas yang sama untuk bergerak dari keadaan transisi ke belakang menuju reaktan atau ke depan menuju produk. Dalam reaksi yang dikatalisis enzim, energi aktivasi keseluruhan reaksi diturunkan ketika enzim menstabilkan perantara keadaan transisi berenergi tinggi. Analog keadaan transisi meniru perantara berenergi tinggi ini tetapi tidak mengalami reaksi kimia yang dikatalisis, dan oleh karena itu dapat mengikat enzim jauh lebih kuat daripada analog substrat atau produk sederhana.
Untuk mendesain analog keadaan transisi, langkah penting adalah penentuan struktur keadaan transisi substrat pada enzim spesifik yang diminati dengan metode eksperimental, misalnya efek isotop kinetik. Selain itu, struktur keadaan transisi juga dapat diprediksi dengan pendekatan komputasi sebagai pelengkap KIE.
Efek isotop kinetik (KIE) adalah pengukuran laju reaksi reaktan berlabel isotop terhadap substrat alami yang lebih umum. Nilai efek isotop kinetik merupakan rasio dari angka pergantian dan mencakup semua tahapan reaksi. Nilai isotop kinetik intrinsik berasal dari perbedaan lingkungan vibrasi ikatan atom dalam reaktan pada keadaan dasar dengan lingkungan keadaan transisi atom tersebut.[3] Melalui efek isotop kinetik, banyak wawasan dapat diperoleh mengenai seperti apa keadaan transisi dari reaksi yang dikatalisis enzim dan memandu pengembangan analog keadaan transisi.
Pendekatan komputasi telah dianggap sebagai alat yang berguna untuk menjelaskan mekanisme kerja enzim.[4] Mekanika molekuler sendiri tidak dapat memprediksi transfer elektron yang merupakan dasar reaksi organik, tetapi simulasi dinamika molekuler memberikan informasi yang cukup dengan mempertimbangkan fleksibilitas protein selama reaksi katalitik. Metode pelengkapnya adalah kombinasi metode simulasi mekanika molekuler/mekanika kuantum (QM/MM).[5] Dengan pendekatan ini, hanya atom-atom yang bertanggung jawab atas reaksi enzimatik di wilayah katalitik yang akan ditangani dengan mekanika kuantum, dan atom-atom lainnya ditangani dengan mekanika molekuler.[6]
Setelah menentukan struktur keadaan transisi menggunakan KIE atau simulasi komputasi, penghambat dapat dirancang sesuai dengan struktur keadaan transisi atau intermediet yang telah ditentukan. Tiga contoh berikut mengilustrasikan bagaimana penghambat meniru struktur keadaan transisi dengan mengubah gugus fungsional yang sesuai dengan geometri dan distribusi elektrostatik dari struktur keadaan transisi.

Metiltioadenosina nukleosidase adalah enzim yang mengkatalisis reaksi deadenilasi hidrolitik dari 5'-metiltioadenosina dan S-adenosilhomosisteina. Enzim ini juga dianggap sebagai target penting untuk penemuan obat antibakteri karena penting dalam sistem metabolisme bakteri dan hanya diproduksi oleh bakteri.[7] Mengingat jarak yang berbeda antara atom nitrogen adenina dan karbon anomerik ribosa (lihat diagram di bagian ini), struktur keadaan transisi dapat didefinisikan oleh tahap disosiasi awal atau akhir. Berdasarkan temuan struktur keadaan transisi yang berbeda, Schramm dan rekan kerjanya merancang dua analog keadaan transisi yang meniru keadaan transisi disosiatif awal dan akhir. Analog keadaan transisi awal dan akhir menunjukkan afinitas pengikatan (Kd) masing-masing sebesar 360 dan 140 pM.[8]
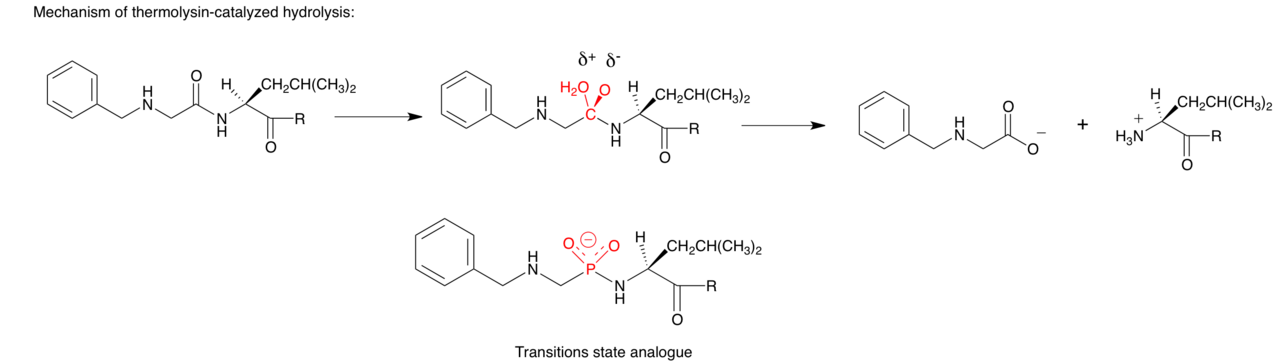
Termolisin adalah enzim yang diproduksi oleh bakteri Bacillus thermoproteolyticus yang mengkatalisis hidrolisis peptida yang mengandung asam amino hidrofobik.[9] Oleh karena itu, ia juga merupakan target untuk agen antibakteri. Mekanisme reaksi enzimatik dimulai dari molekul peptida kecil dan menggantikan molekul air pengikat seng menuju Glu143 dari termolisin. Molekul air kemudian diaktifkan oleh ion seng dan residu Glu143 dan menyerang karbonil karbon untuk membentuk keadaan transisi tetrahedral (lihat gambar). Holden dan rekan kerjanya kemudian meniru keadaan transisi tetrahedral tersebut untuk merancang serangkaian analog peptida fosfonamidat. Di antara analog yang disintesis, R = L-Leu memiliki aktivitas penghambatan paling kuat (Ki = 9,1 nM).[10]

Arginase adalah metaloprotein mangan binuklir yang mengkatalisis hidrolisis L-arginina menjadi L-ornitina dan urea. Arginase juga dianggap sebagai target obat untuk pengobatan asma.[11] Mekanisme hidrolisis L-arginina dilakukan melalui serangan nukleofilik pada gugus guanidino oleh air, sehingga membentuk intermediet tetrahedral. Studi menunjukkan bahwa gugus asam boronat mengadopsi konfigurasi tetrahedral dan berfungsi sebagai penghambat. Selain itu, gugus fungsi sulfonamida juga dapat meniru struktur keadaan transisi.[12] Bukti adanya tiruan asam boronat sebagai penghambat analog keadaan transisi arginase I manusia telah diuraikan melalui struktur kristal sinar-X.[13]