Struktur kimia merupakan informasi penataan atom-atom dan ikatan-ikatan yang membentuk suatu senyawa kimia. Struktur ini dapat digunakan untuk membahas sebuah molekul atau kumpulan atom seperti kristal. Informasi ini termasuk geometri molekul, konfigurasi elektron, dan bahkan struktur kristal.
Sumber: Lihat artikel asli di Wikipedia


Struktur kimia merupakan informasi penataan atom-atom dan ikatan-ikatan yang membentuk suatu senyawa kimia. Struktur ini dapat digunakan untuk membahas sebuah molekul atau kumpulan atom seperti kristal. Informasi ini termasuk geometri molekul, konfigurasi elektron, dan bahkan struktur kristal.[1][2]
Geometri molekul mengacu pada penataan atom dalam ruang tiga dimensi dan umumnya juga melibatkan panjang ikatan dan sudut ikatan di antara atom-atom yang berikatan, sedangkan konfigurasi elektron merupakan deskripsi pengisian orbital dari molekul tersebut.[3][4]
Struktur kimia harus mampu diterapkan untuk menjelaskan struktur molekul dengan baik, dari molekul sederhana seperti gas oksigen (O2) dan nitrogen (N2) hingga yang kompleks seperti protein dan DNA.[5][6]
Penentuan struktur kimia merupakan salah satu kegiatan penting dalam ilmu kimia karena struktur kimia menjadi aspek inti dari ilmu ini.[7]
Terdapat berbagai metode dalam penentuan struktur kimia, masing-masing memiliki kegunaan untuk mempelajari satu atau beberapa aspek dari senyawa tersebut. Seseorang harus mampu membedakan bagian keterikatan antaratom dalam molekul, bagian penataan dalam ruang tiga dimensi (seperti konfigurasi molekul cis-trans atau E-Z dan kiralitas), dan bagian pengukuran nilai dari panjang ikatan, sudut ikatan, dan sebagainya. Maka dari itu, upaya penentuan struktur kimia ini dimulai dari menentukan pola dan jenis ikatan yang terlibat, sebelum mendapatkan struktur tiga dimensi yang lengkap dengan besaran-besarannya.[8]
Metode penentuan struktur umumnya melibatkan metode spektroskopi, yakni metode yang memanfaatkan interaksi antara radiasi elektromagnetik dengan materi. Beberapa peraih Nobel mempopulerkan metode ini untuk mengelusidasi struktur kimia, seperti John Kendrew, Max F. Perutz, dan Dorothy Hodgkin.[2] Beberapa di antaranya adalah sebagai berikut:
Metode untuk mencari keterikatan atom dan struktur elektronik
Metode untuk mencari struktur tiga dimensi:
Begitu struktur kimia dari suatu molekul sudah ditentukan, seseorang dapat membentuk representasinya menggunakan struktur Lewis (untuk keterikatan atom paling sederhana) dan bahkan dapat menggambar struktur tiga dimensi dengan model bola molekuler seperti model bola-dan-pasak atau model ruang terisi.[15]
Begitu struktur kimia dari suatu molekul sudah ditentukan, seseorang dapat menggambarkannya dengan struktur Lewis (untuk keterikatan atom paling sederhana) dan bahkan dapat memprediksi geometri molekulnya. Untuk membangun geometri tersebut, salah satu aspek penting yang perlu ditinjau adalah sifat elektron (dan orbital yang terisi elektron) yang bermuatan negatif. Elektron yang berada pada posisi berdekatan akan mengalami tolakan sehingga geometri molekul paling optimal akan terbentuk apabila tolakan ini minimum.
Inilah yang menjadi landasan teori tolakan pasangan elektron valensi (Valence-Shell Electron Pair Repulsion, VSEPR) sehingga seseorang mampu untuk membuat perkiraan geometri dari sebuah molekul. Pasangan elektron bebas (PEB) akan mengalami tolakan yang lebih besar daripada pasangan elektron yang terlibat dalam ikatan (PEI). Teori ini mampu memberikan pendekatan yang baik dari bentuk dan struktur banyak molekul dan mampu memberikan prediksi yang akurat apabila disempurnakan dengan teori hibridisasi. Tabel di bawah menunjukkan beberapa (prediksi) geometri molekul paling umum dan senyawa-senyawa dengan geometri tersebut.
| Molekul linear | Molekul angular | Molekul planar | Molekul piramidal | Molekul tetrahedral |
|---|---|---|---|---|
 |
 |
 |
 |
|
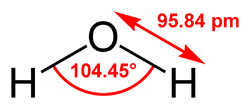
| Molekul karbonil sulfida, SCO | Molekul air, H2O | Molekul boron trifluorida, BF3 | Molekul tiotionil, S2F2 | Molekul silikon tetrafluorida, SiF4 |
| 2 PEI di atom C | 2 PEB + 2 PEI di atom O | 3 PEI di atom B | 1 PEB + 3 PEI di atom S | 4 PEI di atom Si |
| Hibridisasi sp | Hibridisasi sp3 | Hibridisasi sp2 | Hibridisasi sp3 | Hibridisasi sp3 |
Keterangan: Ikatan rangkap dihitung sebagai 1 PEI, tetapi penyederhanaan ini membuat geometri molekul yang diprediksi dengan VSEPR dapat berbeda dengan aslinya.
Apabila geometri molekul sudah ditentukan (diprediksi), senyawa tersebut dapat digambar dalam struktur tiga dimensi dengan model bola molekuler seperti model bola-dan-pasak atau model ruang terisi.[1]
| Molekul | Atom | Ion | Logam |
|---|---|---|---|
 |
 |
 |
 |
| Asam tioasetat, CH3-COSH | Intan, Cn | Tembaga(I) Iodida, CuI2 | Logam |
| Ikatan kovalen molekul | Ikatan kovalen retikuler | Ikatan ionik | Ikatan logam |
Jelas, ketika jumlah atom dalam molekul meningkat, kompleksitas strukturnya meningkat dan metode penentuannya makin sulit. Beberapa di antaranya adalah sebagai berikut.
| Benzena | Heliks α (protein) | DNA | Hemoglobin |
|---|---|---|---|
 |
 |
 |
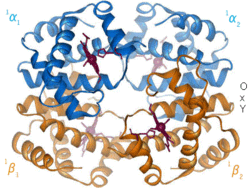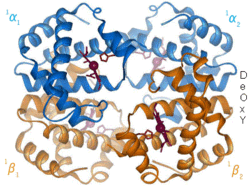 |
| Kekulé (1865)[16][17] | Pauling dan Corey (1951)[18] | Watson dan Crick (1953)[19] | Max F. Perutz (1960)[20][21] |