Teori tumbukan adalah suatu teori yang diusulkan secara independen oleh Max Trautz pada tahun 1916 dan William Lewis pada tahun 1918, yang secara kualitatif menjelaskan bagaimana reaksi kimia terjadi dan bagaimana laju reaksi berbeda bagi reaksi yang berbeda pula. Teori tumbukan menyatakan bahwa ketika partikel reaktan yang sesuai saling bertumbukan, hanya persentase tertentu dari tumbukan yang menyebabkan perubahan kimia yang nyata atau signifikan; perubahan yang berhasil ini disebut sebagai tumbukan yang sukses. Tumbukan yang sukses memiliki energi yang cukup, juga dikenal sebagai energi aktivasi, pada saat tumbukan untuk memutus ikatan yang sudah ada sebelumnya dan membentuk semua ikatan baru. Hal ini menghasilkan produk reaksi. Meningkatkan konsentrasi partikel reaktan atau menaikkan suhu, sehingga menimbulkan lebih banyak benturan dan oleh karena itu banyak tumbukan yang lebih berhasil, meningkatkan laju reaksi.
Sumber: Lihat artikel asli di Wikipedia

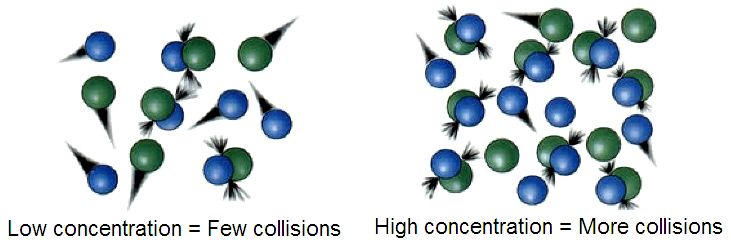
Teori tumbukan adalah suatu teori yang diusulkan secara independen oleh Max Trautz pada tahun 1916[1] dan William Lewis pada tahun 1918, yang secara kualitatif menjelaskan bagaimana reaksi kimia terjadi dan bagaimana laju reaksi berbeda bagi reaksi yang berbeda pula.[2] Teori tumbukan menyatakan bahwa ketika partikel reaktan yang sesuai saling bertumbukan, hanya persentase tertentu dari tumbukan yang menyebabkan perubahan kimia yang nyata atau signifikan; perubahan yang berhasil ini disebut sebagai tumbukan yang sukses. Tumbukan yang sukses memiliki energi yang cukup, juga dikenal sebagai energi aktivasi, pada saat tumbukan untuk memutus ikatan yang sudah ada sebelumnya dan membentuk semua ikatan baru. Hal ini menghasilkan produk reaksi. Meningkatkan konsentrasi partikel reaktan atau menaikkan suhu, sehingga menimbulkan lebih banyak benturan dan oleh karena itu banyak tumbukan yang lebih berhasil, meningkatkan laju reaksi.
Bila katalis terlibat dalam tumbukan antara molekul reaktan, diperlukan sedikit energi agar terjadi perubahan kimiawi, dan karenanya lebih banyak tumbukan memiliki energi yang cukup untuk reaksi terjadi. Laju reaksi karenanya meningkat.
Teori tumbukan sangat erat kaitannya dengan kinetika kimia.
Konstanta laju bagi suatu reaksi fase gas bimolekular, sebagaimana diprediksi oleh teori tumbukan adalah:
di mana:
Frekuensi tumbukan adalah:
di mana: