Dalam kimia organik, gugus toluenasulfonil (disebut juga dengan gugus tosil, disingkat Ts atau Tos) adalah gugus fungsional univalen dengan rumus kimia −SO2−C6H4−CH3. Gugus ini terdiri dari gugus tolil (−C6H4−CH3) yang terikat pada gugus sulfonil (−SO2−) dengan valensi terbuka pada belerang. Gugus ini biasanya berasal dari senyawa tosil klorida (CH3C6H4SO2Cl, disingkat TsCl), yang membentuk ester dan amida dari asam toluenasulfonat (CH3C6H4SO2OH, disingkat TsOH). Orientasi para yang diilustrasikan (p-toluenasulfonil) adalah yang paling umum, dan menurut konvensi tosil tanpa awalan mengacu pada gugus p-toluenasulfonil.
Sumber: Lihat artikel asli di Wikipedia
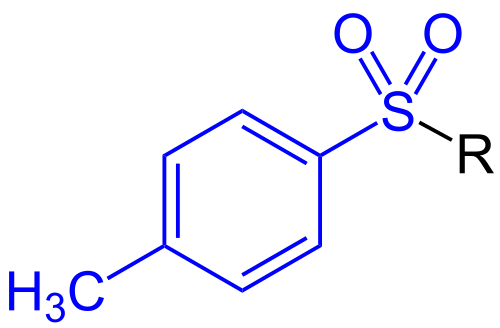


Dalam kimia organik, gugus toluenasulfonil (disebut juga dengan gugus tosil, disingkat Ts atau Tos[nb 1]) adalah gugus fungsional univalen dengan rumus kimia −SO2−C6H4−CH3. Gugus ini terdiri dari gugus tolil (−C6H4−CH3) yang terikat pada gugus sulfonil (−SO2−) dengan valensi terbuka pada belerang. Gugus ini biasanya berasal dari senyawa tosil klorida (CH3C6H4SO2Cl, disingkat TsCl), yang membentuk ester dan amida dari asam toluenasulfonat (CH3C6H4SO2OH, disingkat TsOH). Orientasi para yang diilustrasikan (p-toluenasulfonil) adalah yang paling umum, dan menurut konvensi tosil tanpa awalan mengacu pada gugus p-toluenasulfonil.
Terminologi tosil diusulkan oleh ahli kimia Jerman yakni Kurt Hess dan Robert Pfleger pada tahun 1933 berdasarkan pola tritil[1] dan diadopsi dalam bahasa Inggris mulai tahun 1934.[2]
Gugus toluenasulfonat (atau tosilat) mengacu pada gugus −O−SO2C6H4CH3 (–OTs), dengan oksigen tambahan yang terikat pada belerang dan valensi terbuka pada oksigen.[3] Dalam nama kimia, istilah "tosilat" dapat merujuk pada garam yang mengandung anion asam p-toluenasulfonat (TsO−M+, misalnya natrium p-toluenasulfonat), atau dapat merujuk pada ester asam p-toluenasulfonat (TsOR, R = gugus organil).
Untuk reaksi SN2, alkohol alkil juga dapat diubah menjadi alkil tosilat, seringkali melalui penambahan tosil klorida. Dalam reaksi ini, pasangan elektron bebas oksigen alkohol menyerang belerang dari tosil klorida, menggantikan klorida dan membentuk tosilat dengan mempertahankan stereokimia reaktan. Ini berguna karena alkohol merupakan gugus pergi yang buruk dalam reaksi SN2, berbeda dengan gugus tosilat. Transformasi alkohol alkil menjadi alkil tosilat memungkinkan terjadinya reaksi SN2 dengan adanya nukleofil yang baik.
Gugus tosil dapat berfungsi sebagai gugus pelindung dalam sintesis organik. Alkohol dapat diubah menjadi gugus tosilat sehingga tidak bereaksi. Gugus tosilat kemudian dapat diubah kembali menjadi alkohol. Penggunaan gugus fungsional ini dicontohkan dalam sintesis organik obat tolterodin, di mana salah satu langkahnya adalah gugus fenol dilindungi sebagai tosilatnya dan alkohol primer sebagai nosilatnya. Yang terakhir merupakan gugus lepas untuk substitusi oleh diisopropilamina:[4][nb 2]
Gugus tosil juga berguna sebagai gugus pelindung untuk amina. Struktur sulfonamida yang dihasilkan sangat stabil. Gugus ini dapat dideproteksi untuk mengungkapkan amina menggunakan kondisi reduktif atau asam kuat.[5]

Gugus tosil (disingkat Ts) umumnya digunakan sebagai gugus pelindung untuk amina dalam sintesis organik.

Senyawa yang sangat terkait dengan tosilat adalah nosilat dan brosilat, yang masing-masing merupakan singkatan dari o- atau p-nitrobenzenasulfonat dan p-bromobenzenasulfonat.