Sumber: Lihat artikel asli di Wikipedia


Senyawa aromatik atau arena adalah senyawa organik "dengan kimia yang dicirikan oleh benzena" dan "terkonjugasi secara siklik."[1] Kata "aromatik" berasal dari pengelompokan molekul berdasarkan bau di masa lalu, sebelum sifat kimia umumnya dipahami. Definisi senyawa aromatik saat ini tidak memiliki hubungan dengan baunya. Senyawa aromatik sekarang didefinisikan sebagai senyawa siklik yang memenuhi aturan Hückel. Senyawa aromatik memiliki sifat umum berikut:
Arena biasanya dibagi menjadi dua kategori, yakni benzoid yang mengandung turunan benzena dan mengikuti model cincin benzena, dan non-benzoid yang mengandung turunan siklik aromatik lainnya. Senyawa aromatik umumnya digunakan dalam sintesis organik dan terlibat dalam banyak jenis reaksi, baik penambahan maupun penghilangan, serta penjenuhan dan dearomatisasi.
Heteroarena adalah senyawa aromatik, di mana setidaknya satu gugus metina atau vinilena (-C= atau -CH=CH-) digantikan oleh heteroatom: oksigen, nitrogen (azaarena), atau belerang.[3] Contoh senyawa non-benzena dengan sifat aromatik adalah furan, senyawa heterosiklik dengan cincin beranggota lima yang mencakup satu atom oksigen, dan piridina, senyawa heterosiklik dengan cincin beranggota enam yang mengandung satu atom nitrogen. Hidrokarbon tanpa cincin aromatik disebut "alifatik". Kira-kira setengah dari senyawa yang dikenal pada tahun 2000 digambarkan sebagai aromatik sampai batas tertentu.[4]
Senyawa aromatik tersebar luas di alam dan industri. Hidrokarbon aromatik industri utama adalah benzena, toluena, xilena yang disebut "BTX". Banyak biomolekul memiliki gugus fenil termasuk yang disebut asam amino aromatik.


Benzena (C6H6) adalah hidrokarbon aromatik paling sederhana, dan merupakan yang pertama didefinisikan sebagai demikian. Sifat ikatannya pertama kali dikenali secara independen oleh Josef Loschmidt dan August Kekulé pada abad ke-19.[6] Setiap atom karbon dalam siklus heksagonal memiliki empat elektron untuk dibagi. Satu elektron membentuk ikatan sigma dengan atom hidrogen, dan satu digunakan dalam ikatan kovalen dengan masing-masing dari dua karbon tetangga. Ini menyisakan enam elektron, yang dibagi secara merata di sekitar cincin dalam orbital molekul pi terdelokalisasi seukuran cincin itu sendiri. Ini mewakili sifat ekuivalen dari enam ikatan karbon-karbon yang semuanya ber[[orde ikatan}] 1,5. Kesetaraan ini juga dapat dijelaskan oleh bentuk resonansi. Elektron divisualisasikan mengambang di atas dan di bawah cincin, dengan medan elektromagnetik yang dihasilkannya bertindak untuk menjaga cincin tetap datar.[5]
Simbol lingkaran untuk aromatisitas diperkenalkan oleh Sir Robert Robinson dan muridnya yakni James Armit pada tahun 1925, dan dipopulerkan mulai tahun 1959 oleh buku teks kimia organik Morrison & Boyd.[7] Penggunaan simbol yang tepat masih diperdebatkan: beberapa publikasi menggunakannya untuk sistem π siklik apa pun, sementara yang lain hanya menggunakannya untuk sistem π yang mematuhi aturan Hückel. Beberapa berpendapat bahwa, agar tetap sesuai dengan usulan awal Robinson, penggunaan simbol lingkaran harus dibatasi pada sistem 6 elektron π monosiklik. Dengan cara ini, simbol lingkaran untuk ikatan enam pusat enam elektron dapat dibandingkan dengan simbol Y untuk ikatan tiga-pusat dua-elektron.[8]

Turunan benzena memiliki satu hingga enam substituen yang terikat pada inti benzena pusat.[2] Contoh senyawa benzena dengan hanya satu substituen adalah fenol, yang membawa gugus hidroksil, dan toluena dengan gugus metil. Ketika terdapat lebih dari satu substituen pada cincin, hubungan spasialnya menjadi penting sehingga pola substitusi arena orto, meta, dan para dirancang. Ketika bereaksi membentuk turunan benzena yang lebih kompleks, substituen pada cincin benzena dapat digambarkan sebagai teraktivasi atau terdeaktivasi, yang masing-masing merupakan pendonor elektron dan penarik elektron. Aktivator dikenal sebagai pengarah orto-para, dan deaktivator dikenal sebagai pengarah meta. Setelah bereaksi, substituen akan ditambahkan pada posisi orto, para, atau meta, tergantung pada arah substituen saat ini untuk menghasilkan turunan benzena yang lebih kompleks, seringkali dengan beberapa isomer. Aliran elektron yang mengarah ke re-aromatisasi merupakan kunci untuk memastikan stabilitas produk tersebut.[9]
Sebagai contoh, terdapat tiga isomer untuk kresol karena gugus metil dan gugus hidroksil (keduanya merupakan pengarah orto-para) dapat ditempatkan bersebelahan (orto), satu posisi terpisah (meta), atau dua posisi terpisah (para). Mengingat bahwa baik gugus metil maupun gugus hidroksil merupakan pengarah orto-para, isomer orto dan para biasanya lebih disukai.[10]
Cincin arena dapat menstabilkan muatan, seperti yang terlihat pada misalnya fenol (C6H5–OH), yang bersifat asam pada gugus hidroksil (OH), karena muatan pada oksigen (alkoksida –O−) sebagian terdelokalisasi ke dalam cincin benzena.
Meskipun arena benzilik umum, senyawa non-benzilik juga sangat penting. Senyawa apa pun yang mengandung bagian siklik yang sesuai dengan aturan Hückel dan bukan turunan benzena dapat dianggap sebagai senyawa aromatik non-benzilik.[5]
Dari anulena yang lebih besar dari benzena, [12]anulena dan [14]anulena adalah senyawa aromatik lemah; dan [18]anulena, Siklooktadekanonaena, bersifat aromatik, meskipun tegangan dalam struktur menyebabkan sedikit penyimpangan dari struktur planar yang tepat, yang diperlukan untuk kategorisasi aromatik.[11] Contoh lain dari arena monosiklik non-benzilik adalah siklopropenil (kation siklopropenium), yang memenuhi aturan Hückel dengan n sama dengan 0. Perlu dicatat, hanya bentuk kationik dari propenil siklik ini yang bersifat aromatik, mengingat netralitas dalam senyawa ini akan melanggar aturan oktet atau aturan Hückel.[12]
Arena monosiklik non-benzilik lainnya termasuk heteroarena yang telah disebutkan sebelumnya yang dapat menggantikan atom karbon dengan heteroatom lain seperti N, O atau S.[5] Contoh umum dari senyawa ini adalah pirola beranggota lima dan piridina beranggota enam, keduanya memiliki nitrogen tersubstitusi.[13]

Hidrokarbon aromatik polisiklik, yang juga dikenal sebagai senyawa aromatik polinuklir (PAH), adalah hidrokarbon aromatik yang terdiri dari cincin aromatik sederhana yang menyatu dan tidak mengandung heteroatom atau membawa substituen.[14] Naftalena adalah contoh paling sederhana dari PAH. PAH terdapat dalam minyak, batu bara, dan endapan tar, dan dihasilkan sebagai produk sampingan dari pembakaran bahan bakar (baik bahan bakar fosil maupun biomassa).[15] Sebagai polutan, PAH menjadi perhatian karena beberapa senyawa telah diidentifikasi sebagai karsinogenik, mutagenik, dan teratogenik.[16][17][18][19] PAH juga ditemukan dalam makanan yang dimasak. Penelitian menunjukkan bahwa kadar PAH yang tinggi ditemukan; misalnya pada daging yang dimasak pada suhu tinggi seperti dipanggang atau dibakar, dan pada ikan asap.[15][16] Mereka juga merupakan molekul kandidat yang baik untuk bertindak sebagai dasar bagi bentuk kehidupan paling awal.[20] Pada grafena, motif PAH diperluas menjadi lembaran 2D yang besar.[21]
Sistem cincin aromatik berpartisipasi dalam banyak reaksi organik.
Dalam substitusi aromatik, satu substituen pada cincin arena, biasanya hidrogen, digantikan oleh reagen lain.[5] Dua jenis utama adalah substitusi elektrofilik aromatik ketika reagen aktif adalah elektrofil, dan substitusi aromatik nukleofilik ketika reagen adalah nukleofil. Dalam substitusi aromatik radikal bebas-nukleofilik, reagen aktif adalah radikal bebas.[22][23]
Contoh substitusi elektrofilik aromatik adalah nitrasi asam salisilat, di mana gugus nitro ditambahkan para terhadap substituen hidroksida:

Substitusi aromatik nukleofilik melibatkan penggantian gugus pergi seperti halida pada cincin aromatik. Cincin aromatik biasanya bersifat nukleofilik, tetapi dengan adanya gugus penarik elektron, senyawa aromatik mengalami substitusi nukleofilik. Secara mekanistik, reaksi ini berbeda dari reaksi SN2 biasa, karena terjadi pada atom karbon trigonal (hibridisasi sp2).[24]

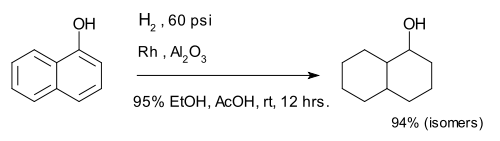
Hidrogenasi arena menghasilkan cincin jenuh. Senyawa 1-naftol direduksi sepenuhnya menjadi campuran isomer dekalin-ol.[25]
Senyawa resorsinol, dihidrogenasi dengan nikel Raney dengan adanya natrium hidroksida berair membentuk enolat yang dialkilasi dengan metil iodida menjadi 2-metil-1,3-sikloheksandion:[26]

Dalam reaksi dearomatisasi, aromatisitas reaktan hilang. Dalam hal ini, dearomatisasi terkait dengan hidrogenasi. Pendekatan klasik adalah reduksi Birch. Metodologi ini digunakan dalam sintesis.[27]

Interaksi arena-arena telah menarik banyak perhatian. Penumpukan pi (juga disebut penumpukan π–π) mengacu pada interaksi pi nonkovalen yang diduga menarik antara ikatan pi cincin aromatik, karena tumpang tindih orbital.[29] Menurut beberapa penulis, penumpukan langsung cincin aromatik ("interaksi sandwich") bersifat tolak-menolak secara elektrostatik.
Yang lebih umum diamati adalah penumpukan berselang-seling (bergeser sejajar) atau interaksi pi-teeing (berbentuk T tegak lurus) yang keduanya bersifat tarik-menarik secara elektrostatik.[30][31] Misalnya, interaksi yang paling umum diamati antara cincin aromatik residu asam amino dalam protein adalah penumpukan berselang-seling diikuti oleh orientasi tegak lurus. Orientasi sandwich relatif jarang.[32]
Susunan pi bersifat tolak-menolak karena menempatkan atom karbon dengan muatan negatif parsial dari satu cincin di atas atom karbon bermuatan negatif parsial lainnya dari cincin kedua dan atom hidrogen dengan muatan positif parsial di atas atom hidrogen lain yang juga membawa muatan positif parsial.[30] Dalam susunan berselang-seling, salah satu dari dua cincin aromatik diimbangi ke samping sehingga atom karbon dengan muatan negatif parsial di cincin pertama ditempatkan di atas atom hidrogen dengan muatan positif parsial di cincin kedua sehingga interaksi elektrostatik menjadi tarik-menarik. Demikian pula, interaksi pi-teeing di mana kedua cincin diorientasikan tegak lurus satu sama lain bersifat tarik-menarik secara elektrostatik karena menempatkan atom hidrogen bermuatan positif parsial dalam jarak dekat dengan atom karbon bermuatan negatif parsial. Penjelasan alternatif untuk preferensi susunan berselang-seling disebabkan oleh keseimbangan antara [[gaya van der Waals|interaksi van der Waals (dispersi tarik-menarik ditambah tolakan Pauli).[33]
Interaksi penumpukan bertingkat dan π-teeing antara cincin aromatik ini penting dalam penumpukan nukleobasa dalam molekul DNA dan RNA, pelipatan protein, sintesis terarah templat, ilmu material, dan pengenalan molekuler. Meskipun istilah penumpukan pi banyak digunakan dalam literatur ilmiah, tidak ada justifikasi teoritis untuk penggunaannya.[30]

Dimer benzena adalah sistem prototipe untuk studi penumpukan pi, dan secara eksperimental terikat oleh 8–12 kJ/mol (2–3 kkal/mol) dalam fase gas dengan pemisahan 4,96 Å antara pusat massa untuk dimer berbentuk T. Kristalografi sinar-X mengungkapkan konfigurasi tegak lurus dan paralel yang bergeser untuk banyak senyawa aromatik sederhana.[34] Geometri paralel atau tegak lurus yang serupa diamati dalam survei struktur kristal protein sinar-X resolusi tinggi di Protein Data Bank.[35] Analisis asam amino aromatik fenilalanina, tirosin, histidina, dan triptofan menunjukkan bahwa dimer rantai samping ini memiliki banyak interaksi penstabil pada jarak yang lebih besar dari jari-jari van der Waals rata-rata.[32]

Energi ikatan relatif dari tiga geometri dimer benzena dapat dijelaskan oleh keseimbangan gaya kuadrupol/kuadrupol dan gaya dispersi London. Meskipun benzena tidak memiliki momen dipol, ia memiliki momen kuadrupol yang kuat.[36] Dipol C–H lokal berarti bahwa ada muatan positif pada atom-atom dalam cincin dan muatan negatif yang sesuai yang mewakili awan elektron di atas dan di bawah cincin. Momen kuadrupol dibalik untuk heksafluorobenzena karena elektronegativitas fluorin. Dimer benzena dalam konfigurasi sandwich distabilkan oleh gaya dispersi London tetapi tidak stabil karena interaksi tolak-menolak kuadrupol/kuadrupol. Dengan menggeser salah satu cincin benzena, konfigurasi paralel yang bergeser mengurangi interaksi tolak-menolak ini dan menjadi stabil. Polarisabilitas besar cincin aromatik menyebabkan interaksi dispersif sebagai kontribusi utama terhadap efek penumpukan. Hal ini memainkan peran utama dalam interaksi nukleobasa, misalnya dalam DNA.[37] Konfigurasi berbentuk T memiliki interaksi kuadrupol/kuadrupol yang menguntungkan, karena kuadrupol positif dari satu cincin benzena berinteraksi dengan kuadrupol negatif dari cincin benzena lainnya. Cincin benzena berada pada jarak terjauh dalam konfigurasi ini, sehingga interaksi kuadrupol/kuadrupol yang menguntungkan jelas mengimbangi berkurangnya gaya dispersi.
Menurut salah satu model, substituen penarik elektron menurunkan kuadrupol negatif dari cincin aromatik dan dengan demikian mendukung konformasi paralel yang bergeser dan sandwich. Sebaliknya, gugus pendonor elektron meningkatkan kuadrupol negatif, yang dapat menstabilkan konfigurasi berbentuk T dengan geometri yang tepat.[38] Mereka menggunakan model matematika sederhana berdasarkan muatan atom sigma dan pi, orientasi relatif, dan interaksi van der Waals untuk secara kualitatif menentukan bahwa elektrostatika dominan dalam efek substituen.[39]

Hunter dkk. menerapkan siklus mutan ganda kimia yang lebih canggih dengan "ritsleting" berikatan hidrogen pada masalah efek substituen dalam interaksi penumpukan pi pada protein.[40][41] Namun, penulis mencatat bahwa interaksi langsung dengan substituen cincin, yang dibahas di bawah ini, juga memberikan kontribusi penting. Memang, interaksi kedua faktor ini dapat menghasilkan perilaku interaksi penumpukan pi yang rumit yang bergantung pada substituen dan geometri.
Beberapa bukti eksperimental dan komputasi menunjukkan bahwa interaksi penumpukan pi tidak diatur terutama oleh efek elektrostatik.[42][43]
Kontribusi relatif penumpukan pi telah dibuktikan oleh komputasi.[44][45][46] Tren berdasarkan substituen pendonor atau penarik elektron dapat dijelaskan oleh istilah pertukaran-tolakan dan dispersi.[47]

Keseimbangan torsi molekuler dari ester aril dengan dua keadaan konformasi.[48] Keadaan terlipat memiliki interaksi penumpukan pi yang terdefinisi dengan baik dengan geometri berbentuk T, sedangkan keadaan tidak terlipat tidak memiliki interaksi aril–aril. Pergeseran kimia NMR dari kedua konformasi berbeda dan dapat digunakan untuk menentukan rasio kedua keadaan, yang diinterpretasikan sebagai ukuran gaya intramolekuler. Para penulis melaporkan bahwa preferensi untuk keadaan terlipat tidak hanya unik untuk ester aril. Misalnya, ester sikloheksil lebih menyukai keadaan terlipat daripada ester fenil, dan ester tert-butil lebih menyukai keadaan terlipat dengan preferensi yang lebih besar daripada yang ditunjukkan oleh ester aril mana pun. Ini menunjukkan bahwa aromatisitas bukanlah persyaratan ketat untuk interaksi yang menguntungkan dengan cincin aromatik.
Bukti lain untuk interaksi penumpukan pi non-aromatik meliputi studi kritis dalam kimia teoretis, yang menjelaskan mekanisme yang mendasari pengamatan empiris. Grimme melaporkan bahwa energi interaksi dimer yang lebih kecil, yang terdiri dari satu atau dua cincin sangat mirip untuk senyawa aromatik dan jenuh.[49] Temuan ini sangat relevan dengan biologi, dan menunjukkan bahwa kontribusi sistem pi terhadap fenomena seperti nukleobasa bertumpuk mungkin terlalu dilebih-lebihkan. Namun, telah ditunjukkan bahwa interaksi penstabil yang meningkat terlihat untuk dimer aromatik besar. Seperti yang telah disebutkan sebelumnya, energi interaksi ini sangat bergantung pada geometri. Memang, dimer aromatik besar hanya distabilkan relatif terhadap rekan jenuhnya dalam geometri sandwich, sementara energinya serupa dalam interaksi berbentuk T.

Pendekatan yang lebih langsung untuk memodelkan peran aromatisitas diambil oleh Bloom dan Wheeler.[50] Para penulis membandingkan interaksi antara benzena dan 2-metilnaftalena atau isomer non-aromatiknya, yakni 2-metilen-2,3-dihidronaftalena. Senyawa terakhir ini menyediakan cara untuk mempertahankan jumlah elektron-p, namun menghilangkan efek delokalisasi. Anehnya, energi interaksi dengan benzena lebih tinggi untuk senyawa non-aromatik, menunjukkan bahwa lokalisasi ikatan pi menguntungkan dalam interaksi penumpukan pi. Para penulis juga mempertimbangkan pemisahan homodesmotik benzena menjadi etilena dan 1,3-butadiena dan membandingkan interaksi ini dalam sandwich dengan benzena. Perhitungan mereka menunjukkan bahwa energi interaksi antara benzena dan benzena homodesmotik lebih tinggi daripada dimer benzena baik dalam konformasi sandwich maupun paralel yang bergeser, sekali lagi menyoroti keuntungan dari interaksi ikatan pi yang terlokalisasi. Hasil ini sangat menunjukkan bahwa aromatisitas tidak diperlukan untuk interaksi pi stacking dalam model ini.
Bahkan dengan bukti ini, Grimme menyimpulkan bahwa pi stacking memang ada.[49] Namun, ia memperingatkan bahwa cincin yang lebih kecil, khususnya yang dalam konformasi berbentuk T, tidak berperilaku secara signifikan berbeda dari pasangan jenuhnya, dan bahwa istilah tersebut harus ditentukan untuk cincin yang lebih besar dalam konformasi bertumpuk yang tampaknya menunjukkan efek elektron pi kooperatif.